题目内容
|
下列每组物质中含有化学键类型相同的是 | |
| [ ] | |
A. |
NaCl、HCl、H2O、NaOH |
B. |
Cl2、Na2S、HCl、SO2 |
C. |
HBr、CO2、H2O、CS2 |
D. |
Na2O2、H2O2、H2O、O3 |
答案:C
解析:
解析:
|
解此类题目的关键在于弄清各类化学键的形成本质.离子键是由阴、阳离子相互作用形成的,非极性键是由同种元素原子形成的共价键,极性键是由不同种元素原子形成的共价键.A组中NaCl与NaOH中含有离子键,而HCl和H2O中只有共价键,NaOH中既含有离子键又含有共价键;B组中Cl2、HCl、SO2中只含共价键,而Na2S中只含离子键;而C组中均只含有共价键;D组中Na2O2含离子键、共价键,H2O2、H2O、O3中只含共价键,故C正确. |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
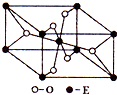 已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B二种元素组成的原子个数比为1:1的化合物N是常见的有机溶剂.E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同.
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍.A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B二种元素组成的原子个数比为1:1的化合物N是常见的有机溶剂.E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同.
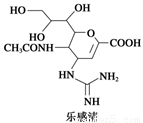

 )存在于我国盛产的八角茴香中。关于莽草酸性质的描述,下列说法正确的是( )
)存在于我国盛产的八角茴香中。关于莽草酸性质的描述,下列说法正确的是( )