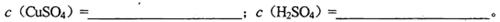题目内容
硫酸铜在工农业生产和生活中都有重要的应用。请回答下列问题:
(1)铜与浓硫酸共热是制备硫酸铜的方法之一,写出反应的化学方程式:__________________。但该反应生成的气体污染环境。为避免环境污染,可在铜粉与稀硫酸的混合物中通入热空气,反应的总化学方程式为____________________。
(2)将铜粉置于稀硫酸中不发生反应,加入双氧水,则铜粉可逐渐溶解。写出反应的离子方程式:____________________。
(3)将适量稀硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶可得到硫酸铜晶体。为了节约原料,H2SO4和HNO3的物质的量之比最佳为________________。
(4)用惰性电极电解硫酸铜溶液,实验装置如图甲所示。图乙是电解过程中产生气体的总体积V与转移电子的物质的量n(e-)的关系图。
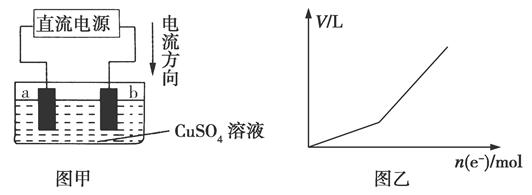
电解过程中,a电极的现象是______________;b电极的电极反应式为____________________。
(1)铜与浓硫酸共热是制备硫酸铜的方法之一,写出反应的化学方程式:__________________。但该反应生成的气体污染环境。为避免环境污染,可在铜粉与稀硫酸的混合物中通入热空气,反应的总化学方程式为____________________。
(2)将铜粉置于稀硫酸中不发生反应,加入双氧水,则铜粉可逐渐溶解。写出反应的离子方程式:____________________。
(3)将适量稀硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶可得到硫酸铜晶体。为了节约原料,H2SO4和HNO3的物质的量之比最佳为________________。
(4)用惰性电极电解硫酸铜溶液,实验装置如图甲所示。图乙是电解过程中产生气体的总体积V与转移电子的物质的量n(e-)的关系图。

电解过程中,a电极的现象是______________;b电极的电极反应式为____________________。
(1)Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O 2Cu+O2+2H2SO4
CuSO4+SO2↑+2H2O 2Cu+O2+2H2SO4 2CuSO4+2H2O
2CuSO4+2H2O
(2)Cu+H2O2+2H+=Cu2++2H2O
(3)3?2
(4)先有红色固体析出,后有无色气泡产生 4OH--4e-=2H2O+O2↑
点拨:本题考查铜及其化合物的性质、电解规律等,意在考查考生对常见物质性质的掌握情况及运用有关原理解决实际问题的能力。
 CuSO4+SO2↑+2H2O 2Cu+O2+2H2SO4
CuSO4+SO2↑+2H2O 2Cu+O2+2H2SO4 2CuSO4+2H2O
2CuSO4+2H2O(2)Cu+H2O2+2H+=Cu2++2H2O
(3)3?2
(4)先有红色固体析出,后有无色气泡产生 4OH--4e-=2H2O+O2↑
点拨:本题考查铜及其化合物的性质、电解规律等,意在考查考生对常见物质性质的掌握情况及运用有关原理解决实际问题的能力。
(1)在热空气存在的情况下,铜相当于被加热,生成氧化铜,然后与稀硫酸反应,此过程中不会产生污染性气体。
(2)双氧水有强氧化性,能将铜氧化为氧化铜。氧化铜能溶于稀硫酸,使反应得以进行。总的化学方程式为Cu+H2O2+H2SO4=CuSO4+2H2O。
(3)3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,Cu(NO3)2+H2SO4=CuSO4+2HNO3(该反应并不能直接发生,是为方便计算而写出),两式叠加消去Cu(NO3)2,得:3Cu+3H2SO4+2HNO3=3CuSO4+2NO↑+4H2O,因此H2SO4和HNO3的物质的量之比最佳为3?2。
(4)由电流方向可知,b电极为阳极,电极反应式始终都是:4OH--4e-=2H2O+O2↑。但图中曲线的斜率有变化,说明起始阶段阴极是Cu2+放电生成铜,然后是H+放电生成了氢气。
(2)双氧水有强氧化性,能将铜氧化为氧化铜。氧化铜能溶于稀硫酸,使反应得以进行。总的化学方程式为Cu+H2O2+H2SO4=CuSO4+2H2O。
(3)3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,Cu(NO3)2+H2SO4=CuSO4+2HNO3(该反应并不能直接发生,是为方便计算而写出),两式叠加消去Cu(NO3)2,得:3Cu+3H2SO4+2HNO3=3CuSO4+2NO↑+4H2O,因此H2SO4和HNO3的物质的量之比最佳为3?2。
(4)由电流方向可知,b电极为阳极,电极反应式始终都是:4OH--4e-=2H2O+O2↑。但图中曲线的斜率有变化,说明起始阶段阴极是Cu2+放电生成铜,然后是H+放电生成了氢气。

练习册系列答案
相关题目
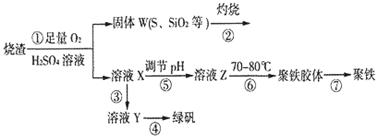
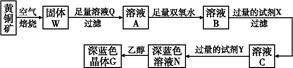
 [Cu(NH3)4]2++2OH-+4H2O,写出该反应的平衡常数表达式: 。
[Cu(NH3)4]2++2OH-+4H2O,写出该反应的平衡常数表达式: 。
 CuSO4和1.0 mol
CuSO4和1.0 mol