题目内容
19.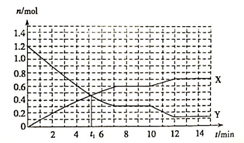 已知反应:A(s)+3B(g)?2C(g)△H<0,在体积为10L的密闭容器中发生反应的过程如图所示,下列说法正确的是( )
已知反应:A(s)+3B(g)?2C(g)△H<0,在体积为10L的密闭容器中发生反应的过程如图所示,下列说法正确的是( )| A. | 前4 min,用A表示反应速率为v(A)=0.005mol/(L•min) | |
| B. | X曲线表示B的物质的量随时间变化的关系 | |
| C. | 第t1min时说明反应达到了平衡 | |
| D. | 第10 min时,可能采取了降温 |
分析 A.根据反应:A(s)+3B(g)?2C(g),A为固体,不能用来表示反应速率;
B.根据物质的量变化量之比等于化学计量数之比判断;
C.反应达到了平衡,反应物生成物的量保持不变;
D.第10 min时,Y的物质的量减小,X的物质的量增大,据此分析.
解答 解:A.反应:A(s)+3B(g)?2C(g),A为固体,不能用来表示反应速率,故A错误;
B.4min时,Y消耗1.2-0.6=0.6,X生成0.4,又方程式中B与C的系数之比=3:2,物质的量变化量之比等于化学计量数之比,则X曲线表示C的物质的量随时间变化的关系,Y曲线表示B的物质的量随时间变化的关系,故B错误;
C.反应达到了平衡,反应物生成物的量保持不变,则t1min时X仍然增大Y减小,所以没有达到平衡,故C错误;
D.第10 min时,Y即B的物质的量减小,X即C的物质的量增大,说明平衡向正反应方向移动,又该反应为放热反应,所以降温可使平衡正向移动,故D正确.
故选D.
点评 本题考查化学平衡以及图象等问题,题目难度中等,注意图象曲线变化的分析,把握外界条件对平衡移动的影响.

练习册系列答案
相关题目
4.一定条件下存在反应:CO(g)+H2O(g)═CO2(g)+H2(g),△H<0.现有三个相同的2L恒容绝热(与外界没有热量交换) 密闭容器I、II、III,在I中充入1mol CO和1mol H2O,在II中充入1mol CO2 和1mol H2,在III中充入2mol CO 和2mol H2O,700℃条件下开始反应.达到平衡时,下列说法正确的是( )
| A. | 容器I、II中正反应速率相同 | |
| B. | 容器I中CO 的物质的量比容器II中的多 | |
| C. | 容器I、III中反应的平衡常数相同 | |
| D. | 容器I中CO 的转化率与容器II中CO2 的转化率之和等于1 |
11.镍是有机合成的重要催化剂.某化工厂有含镍催化剂废品(主要成分是镍,杂质是铁、铝单质及其化合物,少量难溶性杂质).某学习小组设计如图流程利用含镍催化剂废品制备硫酸镍晶体:
几种难溶碱开始沉淀和完全沉淀的pH:
回答下列问题:
(1)溶液①中含有金属的离子是AlO2-.
(2)用离子方程式表示加入双氧水的目的2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)操作b调节溶液范围为3.2~7.1,其目的是除去Fe3+,固体②的化学式为Fe(OH)3.
(4)操作a和c需要共同的玻璃仪器是玻璃棒.上述流程中,防止浓缩结晶过程中Ni2+水解的措施是硫酸过量.
(5)如果加入双氧水量不足或“保温时间较短”,对实验结果的影响是产品中混有绿矾.设计实验证明产品中是否含“杂质”:取少量样品溶于蒸馏水,滴加酸性高锰酸钾溶液,若溶液紫色褪去,则产品中含有亚铁离子.(不考虑硫酸镍影响)
(6)取2.000g硫酸镍晶体样品溶于蒸馏水,用0.2000mol•L-1的EDTA(Na2H2Y)标准溶液滴定至终点,消耗EDTA标准溶液为34.50mL.反应为Ni2++H2Y2?=NiY2?+2H.计算样品纯度为97.0%.(已知,NiSO4•7H2O相对分子质量为281,不考虑杂质反应).

几种难溶碱开始沉淀和完全沉淀的pH:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀 | 3.8 | 2.7 | 7.6 | 7.1 |
| 完全沉淀 | 5.2 | 3.2 | 9.7 | 9.2 |
(1)溶液①中含有金属的离子是AlO2-.
(2)用离子方程式表示加入双氧水的目的2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)操作b调节溶液范围为3.2~7.1,其目的是除去Fe3+,固体②的化学式为Fe(OH)3.
(4)操作a和c需要共同的玻璃仪器是玻璃棒.上述流程中,防止浓缩结晶过程中Ni2+水解的措施是硫酸过量.
(5)如果加入双氧水量不足或“保温时间较短”,对实验结果的影响是产品中混有绿矾.设计实验证明产品中是否含“杂质”:取少量样品溶于蒸馏水,滴加酸性高锰酸钾溶液,若溶液紫色褪去,则产品中含有亚铁离子.(不考虑硫酸镍影响)
(6)取2.000g硫酸镍晶体样品溶于蒸馏水,用0.2000mol•L-1的EDTA(Na2H2Y)标准溶液滴定至终点,消耗EDTA标准溶液为34.50mL.反应为Ni2++H2Y2?=NiY2?+2H.计算样品纯度为97.0%.(已知,NiSO4•7H2O相对分子质量为281,不考虑杂质反应).
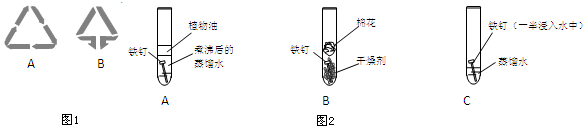
8.只用滴管、试管和水就能鉴别的物质组是( )
| A. | 苯、乙酸、CCl4 | B. | 乙醇、乙酸乙酯、乙酸 | ||
| C. | 苯、硝基苯、溴苯 | D. | 乙醇、甘油、硝基苯 |
 .
.
 碳、氮及其化合物在工农业生产生活中有着重要作用.请回答下列问题:
碳、氮及其化合物在工农业生产生活中有着重要作用.请回答下列问题: