题目内容
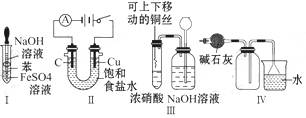
(10分)为了比较氯和碘单质氧化性的强弱,可先制取氯气,并将氯气通入碘化钾淀粉溶液中。下图是本实验所需的仪器和药品:图中A.B.C.D.E.F分别表示玻璃导管或仪器接口。
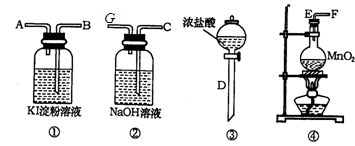
请回答下列问题:
(1)气体流向从左到右。实验前,上述各仪器装置的正确连接顺序是(填各接口的字母符号);D从E处插入烧瓶后,_____________接_____________,_____________接_____________。
(2)写出制备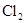 的反应方程式:______ 。
的反应方程式:______ 。
某学生用含0.4molHCl的浓盐酸和足量MnO2反应制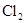 得到的
得到的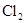 总小于
总小于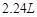 (标况下)为什么?___________________
(标况下)为什么?___________________
(3)实验完成后,装置1中的溶液为_____________色,再向其中滴加足量 溶液颜色是否褪去?_____________(填“是”或“不是”),装置②中NaOH溶液的作用是:______ .
溶液颜色是否褪去?_____________(填“是”或“不是”),装置②中NaOH溶液的作用是:______ .
(4)工业上,可用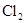 制备漂白粉,请写制备漂白粉的离子反应方程式:
制备漂白粉,请写制备漂白粉的离子反应方程式:
____________ 。

请回答下列问题:
(1)气体流向从左到右。实验前,上述各仪器装置的正确连接顺序是(填各接口的字母符号);D从E处插入烧瓶后,_____________接_____________,_____________接_____________。
(2)写出制备
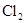 的反应方程式:______ 。
的反应方程式:______ 。某学生用含0.4molHCl的浓盐酸和足量MnO2反应制
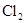 得到的
得到的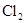 总小于
总小于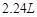 (标况下)为什么?___________________
(标况下)为什么?___________________ (3)实验完成后,装置1中的溶液为_____________色,再向其中滴加足量
 溶液颜色是否褪去?_____________(填“是”或“不是”),装置②中NaOH溶液的作用是:______ .
溶液颜色是否褪去?_____________(填“是”或“不是”),装置②中NaOH溶液的作用是:______ .(4)工业上,可用
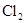 制备漂白粉,请写制备漂白粉的离子反应方程式:
制备漂白粉,请写制备漂白粉的离子反应方程式:____________ 。
(10分)
(1)(2分)F.B.A.C
(2)(2分)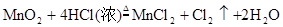
浓盐酸随着反应的进行浓度变稀后,将不再反应, 浓盐酸具有挥发性。(1分)
(3)(3分)蓝 是 吸收剩余的Cl2
(4)(2分)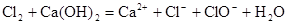
(1)(2分)F.B.A.C
(2)(2分)
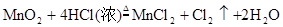
浓盐酸随着反应的进行浓度变稀后,将不再反应, 浓盐酸具有挥发性。(1分)
(3)(3分)蓝 是 吸收剩余的Cl2
(4)(2分)
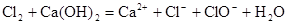
略

练习册系列答案
相关题目
 -
- 要的用途,分别是 和 ;
要的用途,分别是 和 ; 色。该同学还想通过实验分别证实溶质中含有Cu2+、SO42-,请你帮他想想办法,选择适当的试剂(写化学式),并写出其相应的离子方程式。
色。该同学还想通过实验分别证实溶质中含有Cu2+、SO42-,请你帮他想想办法,选择适当的试剂(写化学式),并写出其相应的离子方程式。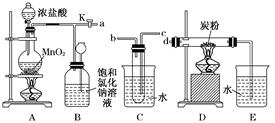
 斗中,然后再注入10 mL CCl4,盖好玻璃塞,振荡,静置于铁架台上,等分层后取上层液
斗中,然后再注入10 mL CCl4,盖好玻璃塞,振荡,静置于铁架台上,等分层后取上层液
 Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如
Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如 下图所示:
下图所示:
 2AlN+3CO中,氧化剂是 。
2AlN+3CO中,氧化剂是 。 CO2+2H2O+4Cu
CO2+2H2O+4Cu 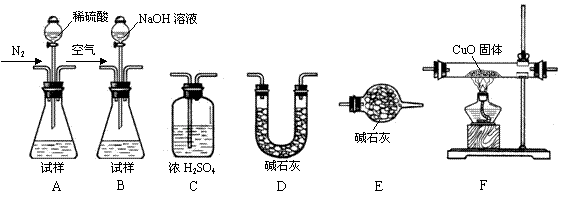 Ⅰ.测定样品中含有少量Al4C3的含量,各装置连接
Ⅰ.测定样品中含有少量Al4C3的含量,各装置连接 的顺序为A→C→F→C→D→E。主要实验步骤
的顺序为A→C→F→C→D→E。主要实验步骤 。
。