��Ŀ����
����Ŀ��A��B��C��D��E������������ͼ��ʾ��ת����ϵ��������A��һ�ֵ���ɫ�Ĺ��塣
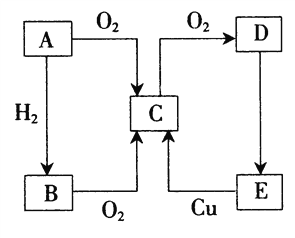
(1)д��B��D�������ʵĻ�ѧʽ��B________��D________��
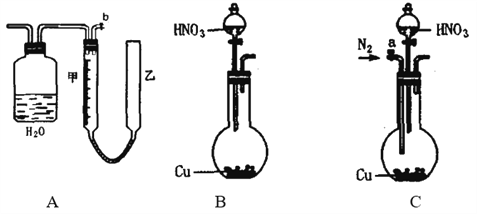
(2)�ٸո��Ƴɵ�ʪ��˿���������ڷ�����C��Ѭ�ƣ�����������C��________���á�
��ʵ�����п���________(���Լ�)������C�Ĵ��ڣ����õ���C��________�ԡ�
(3)Ũ��E��Һ�ڳ�����Ϊ����Һ�壬��E��Һ����ǿ��ˮ�ԡ�ǿ��ˮ�ԡ�ǿ�����ԡ���
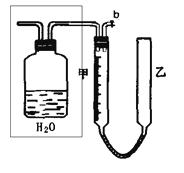
�ٽ�E��Һ���ڷ����ڿ����У�������������_______����������E������_______�ԡ�
��E��Һ������ˮ��ʱ��������������������ʿ���E��Һ�������________��
A��������������������B������(����ǿ��ԭ��)
C��������������������D����������
E��������������������F���⻯��(����ǿ��ԭ��)
G���廯��(����ǿ��ԭ��)
����պ��ŨE��Һ�IJ�������ľ����д�֣��ּ�һ����ͱ�ڣ�˵��ŨE��Һ����________�ԡ�
��ŨE��Һ����ǿ������ʱ���ڼ��ȵ�����������ͭ��̼���ʵȷ�Ӧ����ʵ��E��C��ת������д��E�ֱ���ͭ��̼���ʷ�Ӧ�Ļ�ѧ����ʽ��__________________________________________����ָ��E��ͭ��Ӧʱ�����˱���ǿ�������⣬������ʲô����______________��
��ϡ��E��Һ��������ϴ�ӽ��������ͭ������⣬��д���йصĻ�ѧ����ʽ��______________��
���𰸡� H2S�� SO3 Ư�ס�ɱ������ Ʒ����Һ Ư�� ��С ��ˮ�� CDE ��ˮ 2H2SO4(Ũ)��Cu![]() CuSO4��SO2����2H2O,2H2SO4(Ũ)��C
CuSO4��SO2����2H2O,2H2SO4(Ũ)��C![]() CO2����2SO2����2H2O ���� 3H2SO4��Fe2O3===Fe2(SO4)3��3H2O,2H2SO4��Cu2(OH)2CO3===2CuSO4��CO2����3H2O
CO2����2SO2����2H2O ���� 3H2SO4��Fe2O3===Fe2(SO4)3��3H2O,2H2SO4��Cu2(OH)2CO3===2CuSO4��CO2����3H2O
��������A��B��C��D��E��������������A��һ�ֵ���ɫ�Ĺ��嵥����C�����ܹ�ʹƷ����Һ��ɫ,���ת����ϵ����֪����AΪS��CΪ![]() ��BΪ
��BΪ![]() ��DΪ
��DΪ![]() ��EΪ
��EΪ![]() ��
��
(1)����������B��D�������ʵĻ�ѧʽ�ֱ�Ϊ��H2S��SO3 ����ȷ�𰸣� H2S��SO3��
(2)�ٸո��Ƴɵ�ʪ��˿���������ڷ�����SO2��Ѭ�ƣ�����������SO2��Ư����ɱ���������ã���ȷ�𰸣�Ư�ס�ɱ��������
��ʵ�����п���Ʒ��������SO2�Ĵ��������õ���SO2��Ư��������ȷ����Ʒ����Һ �� Ư�ס�
(3) ����![]() ��Һ���ڷ����ڿ�������Ũ���������ˮ�����������������������������С����������Ũ�����������ˮ�ԣ���ȷ�𰸣���С����ˮ�ԡ�
��Һ���ڷ����ڿ�������Ũ���������ˮ�����������������������������С����������Ũ�����������ˮ�ԣ���ȷ�𰸣���С����ˮ�ԡ�
��Ũ���������ˮ��ʱ�������������Ũ�������백����Ӧ��Ũ�������ǿ���������������������⻯����廯�⣻Ũ������������Ӧ����������Ũ��������������CDE����ȷѡ��CDE��
����պ��Ũ����IJ�������ľ����д�֣��ּ�һ����ͱ�ڣ�˵��Ũ���������ˮ�ԣ���ȷ�𰸣���ˮ��
��Ũ�������ǿ������ʱ���ڼ��ȵ�����������ͭ��Ӧ��������ͭ�����������ˮ����Ӧ�Ļ�ѧ����ʽ��2H2SO4(Ũ)��Cu![]() CuSO4��SO2����2H2O�������ں�ͭ���ȷ�Ӧʱ��һ����Ũ���ᱻ��ԭΪ���������в���Ũ������������ͭ������Ϊ���ԣ��ڼ��ȵ�����������̼��Ӧ���ɶ�����̼�����������ˮ����Ӧ�Ļ�ѧ����ʽ��2H2SO4(Ũ)��C
CuSO4��SO2����2H2O�������ں�ͭ���ȷ�Ӧʱ��һ����Ũ���ᱻ��ԭΪ���������в���Ũ������������ͭ������Ϊ���ԣ��ڼ��ȵ�����������̼��Ӧ���ɶ�����̼�����������ˮ����Ӧ�Ļ�ѧ����ʽ��2H2SO4(Ũ)��C![]() CO2����2SO2����2H2O����ȷ����2H2SO4(Ũ)��Cu
CO2����2SO2����2H2O����ȷ����2H2SO4(Ũ)��Cu![]() CuSO4��SO2����2H2O��2H2SO4(Ũ)��C
CuSO4��SO2����2H2O��2H2SO4(Ũ)��C![]() CO2����2SO2����2H2O�����ԡ�
CO2����2SO2����2H2O�����ԡ�
��ϡ���᳣����ϴ�ӽ��������ͭ������⣬��������������ԣ������ܹ�����������Ӧ������������ˮ����Ӧ����ʽΪ3H2SO4��Fe2O3===Fe2(SO4)3��3H2O�������ܹ����ʽ̼��ͭ��Ӧ��������ͭ��������̼��ˮ����Ӧ����ʽΪ2H2SO4��Cu2(OH)2CO3===2CuSO4��CO2����3H2O����ȷ����3H2SO4��Fe2O3===Fe2(SO4)3��32O��2H2SO4��Cu2(OH)2CO3===2CuSO4��CO2����3H2O��

 ��У���˳�̾�ϵ�д�
��У���˳�̾�ϵ�д� ��У���һ��ͨϵ�д�
��У���һ��ͨϵ�д� �γ̴����Ծ�����100��ϵ�д�
�γ̴����Ծ�����100��ϵ�д�����Ŀ�����з�Ӧ������H2������������
���� | ����Һ | �¶� | |
A | Mg | 0.5molL-1H2SO4 | 20�� |
B | Fe | 1 molL-1HCl | 20�� |
C | Zn | 2 molL-1HCl | 20�� |
D | Mg | 1 molL-1H2SO4 | 30�� |
A.AB.BC.CD.D