题目内容
化学计量在化学中占有重要地位,请回答下列问题。
(1) 0.3molNH3分子中所含原子数与 个H2O分子中所含原子数相等。
(2)含0.4mol Al3+的Al2(SO4) 3中所含的SO42-的物质的量是 。
(3)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为 。
(4)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是 。
(5)某盐混合溶液中含有离子:Na+、Mg2+、Cl-、SO42-,测得Na+、Mg2+和CI-的物质的量浓度依次为:0.2moI·L-l、0.25mol·L-l、0.4mol·L-l,则c (S O42-)= 。
 科学实验活动册系列答案
科学实验活动册系列答案(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H﹤0
CH4(g)+2H2O(g) △H﹤0
则升高温度平衡体系中H2的体积分数将___________;(选填“增大”、“减小”或“不变”)
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
[CO2]/mol·L-1 | [H2]/mol·L-1 | [CH4]/mol·L-1 | [H2O]/mol·L-1 | |
平衡Ⅰ | a | b | c | d |
平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为_________。
(3)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO3- H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。____________________
H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象。____________________
(4)查阅资料获知如下信息:
i.H2CO3:Ki1=4.3×10-7,Ki2=5.6×10-11(以Ki1为主)
ii.标况下,CO2的溶解度为约为1:1
iii.H2O+CO2  H2CO3
H2CO3 
iv. 

 ㏒(6)=0.8
㏒(6)=0.8
请尝试估算:
①饱和二氧化碳溶液中碳酸的物质的量浓度c(H2CO3)约为_______________mol/L;
②饱和二氧化碳溶液中碳酸的电离度α约为_____________。
③正常雨水的pH约为____________。


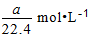 B.
B.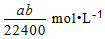
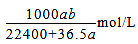 D.
D.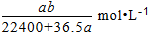
 呈浅黄绿色,说明氯
呈浅黄绿色,说明氯 水中含有Cl2
水中含有Cl2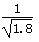 ×10-11mol·L-1
×10-11mol·L-1