题目内容
1.氧化剂和还原剂在生产生活中广泛使用.(1)高锰酸钾和氢溴酸溶液可以发生如下反应:2KMnO4+16HBr=5Br2+2MnBr2+2KBr+8H2O
①其中还原剂为HBr,还原产物为MnBr2
②若有0.8mol还原剂被氧化,则转移电子的物质的量是0.8mol
(2)双氧水H2O2可作为矿业废液消毒剂,可以消除采矿业废液中的氰化物(如KCN,其中N为-3价),化学方程式为:KCN+H2O2+H2O═KHCO3+A↑(已配平)
①生成物A的化学式为NH3
②用双线桥法表示该反应中电子转移的方向和数目:
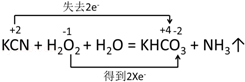
(3)古老但仍然是最有用的制备联氨(N2H4)溶液的方法如下:
1NaClO+2NH3•H2O→1N2H4+1NaCl+3H2O
①请配平上述化学方程式
②NH3•H2O在上述反应中显示出来的性质是B
A.氧化性 B.还原性 C.酸性 D.碱性
(4)人体内所含铁元素以Fe2+ 和Fe3+的形式存在
市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为Fe+2H+═Fe2++H2↑,但Fe2+在酸性条件下很容易被空气中的氧气氧化,写出该反应的离子方程式4Fe2++O2+4H+=4 Fe3++2H2O.
分析 (1)反应2KMnO4+16HBr═5Br2+2MnBr2+2KBr+8H2O中,Br元素化合价升高,Mn元素化合价降低,则反应中KMnO4为氧化剂,HBr为还原剂,根据方程式计算.
(2)①依据化学方程式为KCN+H2O2+H2O=KHCO3+A↑,结合原子个数守恒判断;
②依据化学方程式为:KCN+H2O2+H2O=KHCO3+NH3↑,C由+2价被氧化为KHCO3中的+4,双氧水中的O有-1价降为-2价,所以1molKCN中的C由+2价被氧化为KHCO3中的+4价转移电子数2mol,据此分析;
(3)①反应中Cl的化合价降低,N元素的化合价升高,结合电子守恒和原子守恒配平方程式;
②化合价升高元素在反应中作还原剂,具有还原性.
(4)铁粉在人体胃酸中发生反应生成亚铁离子和氢气;Fe2+在酸性条件下被氧气氧化为铁离子.
解答 解:(1)①反应2KMnO4+16HBr═5Br2+2MnBr2+2KBr+8H2O中,Br元素化合价升高1价,Mn元素化合价降低5价,反应中转移10个电子,反应中KMnO4为氧化剂,MnBr2为还原产物,HBr为还原剂,Br2为氧化产物;
故答案为:HBr;MnBr2;
②HBr为还原剂,若有0.8mol还原剂被氧化,则转移电子的物质的量是0.8mol,故答案为:0.8mol;
(2)①依据化学方程式为:KCN+H2O2+H2O=KHCO3+A↑,由原子个数守恒可知:A中有1个氮原子和3个氢原子,为NH3,故答案为:NH3;
②依据方程式KCN+H2O2+H2O=KHCO3+NH3↑可知,C由+2价被氧化为KHCO3中的+4,双氧水中的O有-1价降为-2价,1molKCN中的C由+2价被氧化为KHCO3中的+4价转移电子数2mol,双线桥表示为 ;
;
故答案为: ;
;
(3)①一水合氨中的氮元素化合价由-3价升高到了-2价,失1mole-电子,次氯酸钠中氯元素化合价由+1价降低到了-1价,则配平方程式为:NaClO+2NH3•H2O=N2H4+NaCl+3H2O,
故答案为:1、2、1、1、3;
②一水合氨中氮元素的化合价升高了,表现了还原性,故答案为:B;
(4)铁粉在人体胃酸中发生反应生成亚铁离子和氢气,离子反应为Fe+2H+=Fe2++H2↑,Fe2+在酸性条件下被氧气氧化为铁离子,其反应的离子方程式为:4Fe2++O2+4H+=4 Fe3++2H2O;
故答案为:Fe+2H+=Fe2++H2↑;4Fe2++O2+4H+=4 Fe3++2H2O.
点评 本题考查氧化还原反应的综合应用,题目难度中等,注意从化合价的角度分析,计算时注意氧化还原反应中氧化剂和还原剂之间得失电子数目相等,表现为化合价升降总数相等.

①2FeCl3+10NaOH+3NaClO═2Na2FeO4+9NaCl+5H2O
②Na2FeO4+2KOH═K2FeO4+2NaOH
下列说法不正确的是( )
| A. | 反应①为氧化还原反应,反应②为复分解反应 | |
| B. | 反应①中NaClO 是氧化剂 | |
| C. | Na2FeO4中Fe为+4价,具有强氧化性,能杀菌消毒 | |
| D. | 若有2 mol FeCl3 发生反应,转移电子的物质的量为 6 mol |
| A. | 把绿豆大的钾投入少量冷水中 | |
| B. | 把Cl2通入FeCl2溶液中 | |
| C. | 把一段打磨过的镁条放入少量冷水中 | |
| D. | 用铂丝蘸取CuCl2溶液于无色火焰上灼烧 |
| A. | 观察纺织品的吸水性 | B. | 测试纺织品的强度 | ||
| C. | 观察纺织品的燃烧的火焰、灰烬 | D. | 测试纺织品的保暖性 |
| A. | 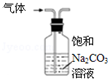 装置可除去CO2中少量的SO2杂质 | B. |  配置一定物质的量浓度的溶液 | ||
| C. | 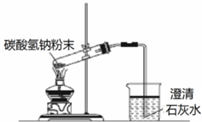 碳酸氢钠受热分解 | D. | 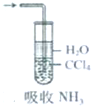 吸收NH3 |
| A. | 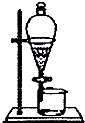 分离碘酒中的碘酒 | B. | 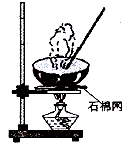 蒸发 | ||
| C. | 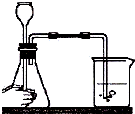 检查装置气密性 | D. |  读取气体体积 |
| A. | 先加入新制氢氧化铜悬浊液,加热;过滤后,调节滤液pH至中性后,在滤液中再加入溴水 | |
| B. | 先加入溴水;后加酸性高锰酸钾溶液 | |
| C. | 先加入酸性高锰酸钾溶液;后加银氨溶液,微热 | |
| D. | 先加入银氨溶液;再另取该物质加入溴水 |