题目内容
【题目】二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体,下列说法中错误的是( ) 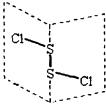
A.S2Cl2的结构式为 Cl﹣S﹣S﹣Cl
B.S2Cl2与水反应时只有S﹣Cl断裂
C.S2Br2含有极性键和非极性键
D.S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O=SO2↑+3S↓+4HCl
【答案】B
【解析】解:A.S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,结合分子结构可知S2Cl2的结构式为Cl﹣S﹣S﹣Cl,故A正确;
B.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,根据结构式判断除了S﹣Cl键断裂外,还有S﹣S键断裂,故B错误;
C.根据S2Cl2的结构式判断,含有Cl﹣S极性键和S﹣S非极性键,故C正确;
D.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),反应的方程式可能为2S2Cl2+2H2O→SO2↑+3S↓+4HCl,故D正确.
故选B.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

