题目内容
硼及其化合物在工农业生产中应用广泛。
(1)基态硼原子的核外电子排布式为__________,有_______种不同能量的电子。
(2)BF3溶于水后.在一定条件下可转化为H3O+·[B(OH)F3]-,该物质中阳离子的空间构型为_____________,阴离子的中心原子轨道采用________杂化;Cu2+也易和NH3形成配离子,已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是_________________________________________________。
(3)与BH4-互为等电子体的分子是_______________(写化学式)。
(4)EminBF4的熔点为12 ℃,在常温下为液体,由有机物阳离子[Emin]+和[BF4]-构成。该物质的晶体属于_________晶体。
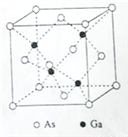
(5)与硼同主族的Ga可与As形成 GaAs晶体,该晶体的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________。Ga和As的摩尔质量分别为MGa g·mol-1 和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿伏伽德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。
根据下列实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
A | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去,2min后,试管里出现凝胶 | 非金属性:Cl>Si |
B | 向滴有甲基橙的AgNO3溶液中滴加KCl溶液,溶液由红色变为黄色 | KCl溶液具有碱性 |
C | 在CuSO4溶液中滴加KI溶液,再加入苯,振荡,有白色沉淀生成,苯层呈紫色 | 白色沉淀可能为CuI |
D | 某溶液滴加盐酸酸化的BaCl2溶液,生成白色沉淀 | 该溶液中可能不含SO42- |
A. A B. B C. C D. D
下列有关物质性质、结构的表述均正确,且存在因果关系的是( )
表述Ⅰ | 表述Ⅱ | |
A | 在水中,NaCl的溶解度比I2的溶解度大 | NaCl晶体中C1—与Na+间的作用力大于碘晶体中分子间的作用力 |
B | 通常条件下,CH4分子比PbH4分子稳定性高 | Pb的原子半径比C的大,Pb与H之间的键能比C与H间的小 |
C | 在形成化合物时,同一主族元素的化合价相同 | 同一主族元素原子的最外层电子数相同 |
D | P4O10、C6H12O6溶于水后均不导电 | P4O10、C6H12O6均属于共价化合物 |
A. A B. B C. C D. D


