题目内容
5.氮化铝(AlN)是一种新型无机材料,广泛应用于电子、陶瓷等工业领域.在一定条件下,AlN可通过反应Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO合成.已知AlN可与NaOH溶液反应放出有刺激性气味的气体.下列叙述正确的是( )| A. | 上述反应中,N2是还原剂,Al2O3是氧化剂 | |
| B. | 上述反应中,每生成1molAlN需转移6mol电子 | |
| C. | AlN属于离子化合物,其中氮元素的化合价为+3 | |
| D. | AlN与NaOH溶液反应的化学方程式为:AlN+NaOH+H2O═NaAlO2+NH3↑ |
分析 化还原反应中化合价升高元素失去电子,所在的反应物是还原剂,对应的产物是氧化产物,化合价降低元素得到电子,所在的反应物是氧化剂,对应的产物是还原产物,化合价升高数目=化合价降低数目=化学反应转移电子数目.
解答 解:A、反应Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO中,氮元素化合价降低,N2是氧化剂,碳元素化合价升高,所以C是还原剂,故A错误;
B、反应Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO中,化合价升高数目=化合价降低数目=化学反应转移电子数目=6,即每生成2molAlN需转移6mol电子,所以每生成1molAlN需转移3mol电子,故B错误;
C、AlN中铝元素显+3价,根据化合价规则,所以氮的化合价为-3,故C错误;
D、AlN与NaOH溶液反应生成偏铝酸钠和氨气,其反应的化学方程式为:AlN+NaOH+H2O═NaAlO2+NH3↑,故D正确.
故选D.
点评 本题考查氧化还原反应,明确元素化合价即可分析解答本题,难度不大,侧重于考查学生的分析能力和对基础知识的应用能力.

练习册系列答案
相关题目
15.下列各组的两种物质在溶液中反应,可用同一离子方程式表示的是( )
| A. | 氢氧化铜与盐酸、氢氧化钡与盐酸 | |
| B. | 石灰石和硝酸溶液、石灰石与盐酸溶液 | |
| C. | BaCO3与HCl溶液、Na2CO3溶液NaHSO4 | |
| D. | 石灰水中通CO2、石灰水中通SO2 |
16.食品安全备受社会关注.下列符合食品安全要求的是( )
| A. | 酱油中添加含铁的营养强化剂 | B. | 饮料中添加塑化剂 | ||
| C. | 用甲醛浸泡海鲜 | D. | 用工业盐腌制腊肉 |
20.下列反应中,氧化与还原在同一元素中进行的是( )
| A. | 3NO2+H2O═2HNO3+NO | B. | Fe+CuSO4═FeSO4+Cu | ||
| C. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | D. | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ |
17.描述CH3-CH═CH-CH═CH-CF3分子结构的叙述中,不正确的是( )
| A. | 1mol该物质最多与2mol氢气加成 | |
| B. | 6个碳原子不可能都在一条直线上 | |
| C. | 6个碳原子有可能都在同一平面上 | |
| D. | 1mol该物质与1mol氢气加成能生成2种不同产物 |
14.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4 LCCl4含有的分子数为NA个 | |
| B. | 500mL 1moL/L的盐酸溶液中含有的HCl分子数为0.5 NA个 | |
| C. | 将1L 2 mol/L的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA个 | |
| D. | 23gNa与O2反应生成Na2O和Na2O2的混合物,转移的电子数为 NA个 |
15.下列物质的化学用语表达正确的是( )
| A. | (CH3)3COH的名称:2,2二甲基乙醇 | B. | 甲烷的球棍模型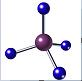 | ||
| C. | 乙醛的结构式:CH3CHO | D. | 四氯化碳分子的电子式: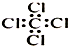 |
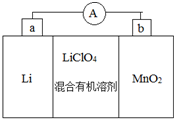 锂锰电池的体积小、性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4.溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答:
锂锰电池的体积小、性能优良,是常用的一次电池.该电池反应原理如图所示,其中电解质LiClO4.溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2.回答: