题目内容
500 mL NaNO3和Cu(NO3)2的混合溶液中c(NO3- )=0.3 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到气体1.12 L(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是
| A.原混合溶液中c(Na+)=0.2 mol·L-1 |
| B.电解后溶液中c(H+)=0.2 mol·L-1 |
| C.上述电解过程中共转移0.4 mol电子 |
| D.电解后得到的Cu的物质的量为0.1 mol |
B
本题考查了电解原理、化学计算等,意在考查考生的分析能力及计算能力。阳极是阴离子放电(??电能力:OH->NO3- ),根据题给信息,阳极一定是OH-放电,生成0.05 mol氧气,转移0.2 mol电子;阴极离子放电能力:Cu2+>H+>Na+,所以Cu2+先放电,然后是H+放电,阴极生成0.05 mol氢气时,转移0.1 mol电子,根据得失电子守恒知,Cu2+转移0.1 mol电子,n(Cu2+)=0.05 mol。所以原溶液中n[Cu(NO3)2]=0.05 mol,n(NO3- )=0.3 mol/L×0.5 L=0.15 mol,n(NaNO3)=0.05 mol。原混合溶液中c(Na+)=0.1 mol·L-1,A项错误;结合以上分析及电解总方程式Cu2++2H2O Cu+H2↑+O2↑+2H+可知,生成0.05 mol Cu、0.05 mol O2、0.05 mol H2和0.1 mol H+,电解后溶液中c(H+)=
Cu+H2↑+O2↑+2H+可知,生成0.05 mol Cu、0.05 mol O2、0.05 mol H2和0.1 mol H+,电解后溶液中c(H+)=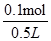 =0.2 mol·L-1,B项正确,D项错误;上述电解过程中共转移0.2 mol电子,C项错误。
=0.2 mol·L-1,B项正确,D项错误;上述电解过程中共转移0.2 mol电子,C项错误。
 Cu+H2↑+O2↑+2H+可知,生成0.05 mol Cu、0.05 mol O2、0.05 mol H2和0.1 mol H+,电解后溶液中c(H+)=
Cu+H2↑+O2↑+2H+可知,生成0.05 mol Cu、0.05 mol O2、0.05 mol H2和0.1 mol H+,电解后溶液中c(H+)=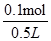 =0.2 mol·L-1,B项正确,D项错误;上述电解过程中共转移0.2 mol电子,C项错误。
=0.2 mol·L-1,B项正确,D项错误;上述电解过程中共转移0.2 mol电子,C项错误。
练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

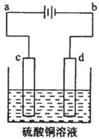

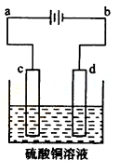
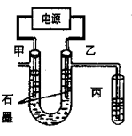
 CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题: