��Ŀ����
����Ŀ��A��B��C��D��E��Ϊ����������Ԫ�أ���ԭ������������������AԪ��ԭ�Ӻ���ֻ��һ�����ӣ�A��C��B��D�ֱ�ͬ���壻B��D��Ԫ��ԭ������֮����A��C��Ԫ��ԭ������֮�͵�2����
��ش��������⣺
��1��������Ԫ����ɵ��������������ڷǵ���ʵ���________(����ĸ)��
A��C2B2 B��DB2 C��E2 D��C2DB3
��2��DԪ����Ԫ�����ڱ��е�λ��Ϊ_______________________________��������C2B���������ӵİ뾶��С��ϵΪ________ �� ________(�����ӷ���)��_____________
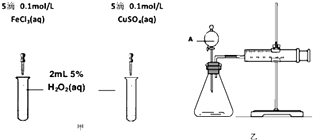
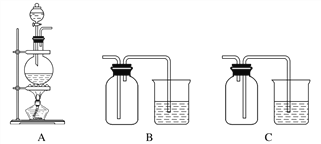
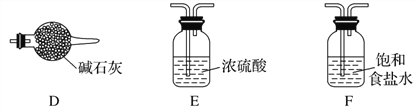
��3��ʵ��������ѡ������װ����ȡ���ռ����������E2���塣
ʵ����Ӧѡ�õ�װ��Ϊ( ) �� ( ) �� ( ) �� ( ) (�������ҵ�����˳����д)��___________
��4�����õ���ʽ��ʾC2D���γɹ��̣�___________________________________
���𰸡� B ����������A�� O2�� > Na�� AFEB ![]()
��������A��B��C��D��E��Ϊ����������Ԫ�أ���ԭ������������������AԪ��ԭ�Ӻ���ֻ��1�����ӣ���AΪH��A��C��B��D�ֱ�ͬ���壻B��D��Ԫ��ԭ������֮����A��C��Ԫ��ԭ������֮�͵�2����CӦΪNa����B��ԭ������Ϊx��D��ԭ������Ϊx+8����2����1+11��=x+x+8�����x=8����BΪO��DΪS��EΪCl��
��1��H2O��HCl��Na2SO3��Ϊ��������ɷ������룬��SO2�������ܵ��룬��ֻ��BΪ�ǵ���ʣ���ȷѡ��B��
��2��DΪS��λ�ڵ�3���ڢ�A�壬������CBAΪNaOH�������Ӽ������ۼ���C2B�����Ӿ�����ͬ�����Ų���ԭ�����������Ӱ뾶С�����Ӱ뾶ΪO2����Na+����ȷ�𰸣��������ڢ�A�� �� O2�� > Na����
��3��װ����ȡ���ռ����������Cl2���壬ѡ��Ũ������������̼����Ʊ�������ʳ��ˮ���Ȼ��⣬Ũ����������ռ���β������������������˳��ΪAFEB����ȷ�𰸣�AFEB��
��4������Ϊ���ӻ�������γɹ���Ϊ��![]() ����ȷ�𰸣�
����ȷ�𰸣�![]() ��
��

 ��ѧ�����ϵ�д�
��ѧ�����ϵ�д� �·Ƿ��̸����100��ϵ�д�
�·Ƿ��̸����100��ϵ�д�