题目内容
I.在一定条件下,反应A(气)+B(气) C(气)+Q达到平衡后,根据下列图象判断
C(气)+Q达到平衡后,根据下列图象判断
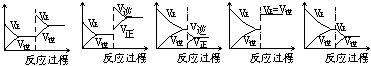
(1)升温,达到新的平衡的是 (2)降压,达到新的平衡的是
(3)减少C的量,移向新平衡的是 (4)增加A的量,移向新平衡的是
(5)使用催化剂,达到平衡的是
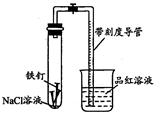
II. CuCl2溶液有时呈黄色,有时呈黄绿色或蓝色,这是因为在CuCl2的水溶液中存在如下
平衡:[Cu(H2O)4]2++4C1一 [CuCl4]2- +4H2O
[CuCl4]2- +4H2O
蓝色 黄色
现欲使溶液由黄色变成黄绿色或蓝色,请写出两种可采用的方法
⑴ ⑵
 C(气)+Q达到平衡后,根据下列图象判断
C(气)+Q达到平衡后,根据下列图象判断
| A. | B. | C. | D. E. |
(3)减少C的量,移向新平衡的是 (4)增加A的量,移向新平衡的是
(5)使用催化剂,达到平衡的是
II. CuCl2溶液有时呈黄色,有时呈黄绿色或蓝色,这是因为在CuCl2的水溶液中存在如下
平衡:[Cu(H2O)4]2++4C1一
 [CuCl4]2- +4H2O
[CuCl4]2- +4H2O蓝色 黄色
现欲使溶液由黄色变成黄绿色或蓝色,请写出两种可采用的方法
⑴ ⑵
I(1)B(2)C(3)E(4)A(5)D
II ⑴ 加硝酸银溶液 ⑵ 加水稀释
II ⑴ 加硝酸银溶液 ⑵ 加水稀释
试题分析:I(1)该反应是放热反应,所以升高温度,平衡向逆反应方向移动,则答案选B。
(2)该反应是体积减小的可逆反应,则降低压强平衡向逆反应方向移动,所以大小C。
(3)减少C的量,平衡向正反应方向移动,答案选E。
(4)增加A的量,平衡向正反应方向移动,答案选A。
(5)使用催化剂,平衡不移动,答案选D。
II.根据方程式可知,欲使溶液由黄色变成黄绿色或蓝色,则应该使平衡向逆反应方向移动,则可采取的措施是加硝酸银溶液或加水稀释。
点评:该题是基础性试题的考查,侧重对学生教材基础知识的巩固和检验。有利于培养学生灵活运用基础知识解决实际问题的能力。该题的关键是明确可逆反应的特点,然后结合题意灵活运用勒夏特列原理即可。

练习册系列答案
相关题目

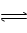 C(g)+D(g)正反应速率增大的措施是 ( )
C(g)+D(g)正反应速率增大的措施是 ( ) 2C(g)+2D(g),在四种不同条件下的反应速率如下,其中反应速率最快的是( )
2C(g)+2D(g),在四种不同条件下的反应速率如下,其中反应速率最快的是( )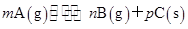
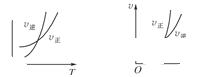
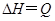 ,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是( )
,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是( )