��Ŀ����
����Ŀ����Ҫ��ش��������⣺ 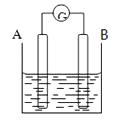
��1������������ָ��ƫ��B����AΪ����BΪ��
��2����������G����ƫת��ͬʱA���������ӣ�B���������٣�CΪ�������Һ����A��B��C�ֱ�Ϊ
A.A��Zn��B��Cu��C��ϡ����
B.A��Cu��B��Zn��C��ϡ����
C.A��Fe��B��Ag��C��ϡAgNO3��Һ
D.A��Ag��B��Fe��C��ϡAgNO3��Һ
��3�����������Һ��ϡ���ᣬ����ͼ��װ�۲쵽A�����ϵ��ܽ⣬B��������ð������A��B�Ľ�����ǿ��Ϊ
��4���κ�һ���Է���������ԭ��Ӧ���������Ϊԭ��أ����õ���з����ķ�ӦΪ��Fe+2FeCl3�T3FeCl2 �� A�缫Ϊ������B�缫Ϊ ��
���𰸡�
��1��������
��2��D
��3��A��B
��4��ͭ��̼��
���������⣺��1����������ָ��������ƫ����ƫ��B������BΪ������AΪ���������Դ��ǣ�����������2����ԭ����У�A�������ӣ�B�����٣�����B��������A��������B�Ļ����Դ���A�Ļ����ԣ������ų�ACѡ� A�������ӣ�˵���н���������Bѡ�������������ǽ�����Dѡ����������������D�������⣮
��ѡD����3�����������Һ��ϡ���ᣬ����ͼ��װ�۲쵽A�����ϵ��ܽ⣬B��������ð�����ܽ��һ��Ϊ�������������ݵ�Ϊ�������������ã����Դ��ǣ�A��B����4�����õ���з����ķ�ӦΪ��Fe+2FeCl3�T3FeCl2 �� A�缫Ϊ����AΪ��������B�缫ѡ���A�����õĽ�����ǽ������壬��A�缫Ϊͭ��̼�������Դ��ǣ�ͭ��̼����

 �������Ͽ�ʱͬ��ѵ��ϵ�д�
�������Ͽ�ʱͬ��ѵ��ϵ�д� �������ͬ����ϰϵ�д�
�������ͬ����ϰϵ�д�