题目内容
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用.完成下列计算:
(1)叠氮化钠(NaN3)受撞击分解产生钠和氮气,故可应用于汽车安全气囊.若78克叠氮化钠完全分解,产生标准状况下氮气
(2)钠-钾合金可在核反应堆中用作热交换液.5.05g钠-钾合金溶于200mL水生成0.075mol氢气.计算溶液中氢氧化钠的物质的量浓度
(3)氢氧化钠溶液处理铝土矿并过滤,得到含铝酸钠的溶液.向该溶液中通入二氧化碳,有下列反应:2NaAl(OH)4+CO2→2Al(OH)3↓+Na2CO3+H2O
己知通入二氧化碳112L(标准状况下),生成的Al(OH)3和Na2CO3的物质的量之比为4:5.若向该溶液中通入的二氧化碳为224L(标准状况下),计算生成的 Al(OH)3和Na2CO3的物质的量的最大值.
(4)为测定某硫酸吸收含氨气废气后,所得铵盐中氮元素的质量分数,现将不同质量的铵盐固体分别加入到50.00mL相同浓度的氢氧化钠溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解).该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量.部分测定结果如下表:
| 铵盐的质量/g | 10.00 | 20.00 | 30.00 | 50.00 |
| 浓硫酸增加的质量/g | m | m | 1.29 | 0 |
该铵盐的成分为
该铵盐中氮元素的质量分数为:
(2)根据金属的质量之和为5.05g及反应中产生的气体来列式计算即可;
(3)先根据生成的Al(OH)3和Na2CO3的物质的量之比为4:5得出溶液中含有氢氧化钠,二氧化碳先与氢氧化钠反应生成碳酸钠,然后二氧化碳与NaAl(OH)4反应生成Al(OH)3和Na2CO3来计算;最后根据当溶液中的二氧化碳与NaAl(OH)4恰好反应生成Al(OH)3和Na2CO3时生成的 Al(OH)3和Na2CO3的物质的量的达最大值;
(4)本反应历程是:OH-首先是和NH4HSO3中的H+反应,随后有多的OH-再和NH4+反应放出氨气,所以随着铵盐的量的增大,NH4HSO3的量也增大,放出的氨气的量会为0,浓硫酸增加的质量就是氨气的质量.第一次和第二次放出的氨气的量是一样的,所以说第一次肯定是OH-的量过量.利用第二次的量计算(因为OH-不足).
2NaN3
| ||
130g 3×22.4L/mol
78g xL
| 130g |
| 78g |
| 3×22.4L/mol |
| xL |
(2)设钠、钾的物质的量分别为x、y,则
2Na+2H2O═2NaOH+H2↑、2K+2H2O═2KOH+H2↑、
x x
| x |
| 2 |
| y |
| 2 |
| x |
| 2 |
| y |
| 2 |
23X+39Y=5.05
解得:x=0.05mol,y=0.1mol,NaOH的物质的量为0.05mol,其物质的量浓度为:
| 0.05mol |
| 0.2L |
(3)根据生成的Al(OH)3和Na2CO3的物质的量之比为4:5得出溶液中含有氢氧化钠,112L二氧化碳的物质的量为:5mol,
2NaOH+CO2→Na2CO3+H2O
2x x x
2NaAl(OH)4+CO2→2Al(OH)3↓+Na2CO3+H2O,
2y y 2y y
| 2y |
| x+y |
| 4 |
| 5 |
x+y=5
解得:x=3,y=2,NaOH的物质的量为6mol,参加反应的NaAl(OH)44mol,
若向该溶液中通入224L二氧化碳,即10mol(标准状况下),当溶液中的二氧化碳与NaAl(OH)4恰好反应生成Al(OH)3和Na2CO3时生成的 Al(OH)3和Na2CO3的物质的量的达最大值.
2NaOH+CO2=Na2CO3+H2O
6mol 3mol 3mol
2NaAl(OH)4+CO2=2Al(OH)3↓+Na2CO3+H2O
7mol 14mol 7mol
生成的 Al(OH)3和Na2CO3的物质的量的最大值分别为14mol、10 mol,
答:生成的 Al(OH)3和Na2CO3的物质的量的最大值分别为14mol、10 mol;
(4)从吸收塔出来的气体用一定量氨水吸收,得到的铵盐产品是(NH4)2SO4和NH4HSO4的混合物;本反应历程是:OH-首先是和NH4HSO4中的H+反应,随后有多的OH-再和NH4+反应放出氨气,所以随着铵盐的量的增大,NH4HSO4的量也增大,放出的氨气的量会为0.
由题知铵盐质量为30.00g时,产生0.076mol NH3.该铵盐中NH4HSO4先与NaOH溶液反应,2NH4HSO4+2NaOH=(NH4)2SO4+Na2SO4+H2O,只有当NH4HSO4中的H+消耗完全后,NH4+才能与NaOH溶液反应产生NH3,NH4++OH-=NH3↑+H2O.据此判断铵盐质量为10.00g时NaOH溶液过量,铵盐质量为20.00g和30.00g时,消耗的NaOH质量相等.
设10.00g铵盐中NH4HSO4 与(NH4)2SO4的物质的量分别为X、Y,则有:
| 铵盐质量/g | 10.00 | 20.00 | 30.00 | 40.00 |
| 含NH4HSO4、(NH4)2SO4/mol | X、Y | 2X、2Y | 3X、3Y | 4X、4Y |
| 产生NH3/mol | X+2Y | X+2Y | 0.076mol | 0 |
| 消耗NaOH/mol | 2X+2Y | 3X+2Y | 3X+0.076mol | 3X+0.076mol |
则该铵盐中氮元素的质量分数
| (0.043mol+0.076mol)×14g/mol |
| 10g |
即铵盐中氮元素的质量分数为16.7%,故答案为:(NH4)2SO4和NH4HSO4;16.7%.

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案完成下列计算:
(1)将4.6g金属钠投入100克水中,充分反应.已知:2Na+2H2O→2NaOH+H2↑
①生成标准状况下氢气
②求反应后溶液中NaOH的质量分数
(2)将10g CO和CO2的混合气体,通过装有足量过氧化钠的干燥管,反应后干燥管的总质量增加了5.6g.
已知:2Na2O2+2CO2→2Na2CO3+O2,求原混合气体中CO2的质量分数.计算过程:
(3)NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:
Na2CO3+nH2O→Na2CO3?nH2O(n为平均值,n≤10).
取没有妥善保管已部分变质的NaHCO3样品A 9.16g,溶于水配成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如下表.(不计溶于水的CO2气体)
| 盐酸体积(mL) | 8 | 15 | 20 | 50 | x | 120 | 150 |
| 生成CO2体积(mL) | 0 | 112 | 224 | 896 | 2240 | 2240 | 2240 |
Na2CO3+HCl→NaHCO3+NaCl NaHCO3+HCl→NaCl+CO2↑+H2O
试求:
①滴入稀盐酸的物质的量浓度为:
②当加入盐酸后,生成CO2体积不再增加时,x的最小值为
③部分变质后样品A中:NaHCO3的物质的量;Na2CO3?nH2O的物质的量以及n值.计算过程:
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。
完成下列计算:
57.叠氮化钠(NaN3)受撞击完全分解产生钠和氮气,故可应用于汽车安全气囊。若产生40.32 L(标准状况下)氮气,至少需要叠氮化钠___g。
58.钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。
(1)计算溶液中氢氧根离子的物质的量浓度(忽略溶液体积变化)。
(2)计算并确定该钠-钾合金的化学式。
59.氢氧化钠溶液处理铝土矿并过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应:
2NaAl(OH)4+CO2→2Al(OH)3↓ +Na2CO3+H2O
己知通入二氧化碳336 L(标准状况下),生成24 mol Al(OH)3和15 mol Na2CO3,若通入溶液的二氧化碳为112L(标准状况下),计算生成的Al(OH)3和Na2CO3的物质的量之比。
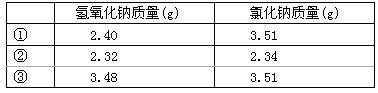
60.常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失。
|
| 氢氧化钠质量(g) | 氯化钠质量(g) |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
上述实验①②③所用氢氧化钠均不含杂质,且实验数据可靠。通过计算,分析和比较上表3组数据,给出结论。
钠是活泼的碱金属元素,钠及其化合物在生产和生活中有广泛的应用。
完成下列计算:
(1)叠氮化钠(NaN3)受撞击分解产生钠和氮气,故可应用于汽车安全气囊。若78克叠氮化钠完全分解,产生标准状况下氮气___________________L 。
(2)钠-钾合金可在核反应堆中用作热交换液。5.05 g钠-钾合金溶于200 mL水生成0.075 mol氢气。计算溶液中氢氧化钠的物质的量浓度______________________(忽略液体体积变化)。
(3)氢氧化钠溶液处理铝土矿并过滤,得到含铝酸钠的溶液。向该溶液中通入二氧化碳,有下列反应: 2NaAl(OH)4+CO2→2Al(OH)3↓+Na2CO3+H2O。己知通入二氧化碳112 L(标准状况下),生成的Al(OH)3和Na2CO3的物质的量之比为4:5。若向该溶液中通入的二氧化碳为224L(标准状况下),计算生成的 Al(OH)3和Na2CO3的物质的量的最大值。
(4)为测定某硫酸吸收含氨气废气后,所得铵盐中氮元素的质量分数,现将不同质量的铵盐固体分别加入到50.00mL相同浓度的氢氧化钠溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。部分测定结果如下表:
|
铵盐的质量/g |
10.00 |
20.00 |
30.00 |
50.00 |
|
浓硫酸增加的质量/g |
m |
m |
1.29 |
0 |
试回答:
该铵盐的成分为_______________________________。
该铵盐中氮元素的质量分数为:_______________________________(须列式计算)。