题目内容
 (2012?石家庄模拟)科学家一直致力于“人工固氮”的方法研究.
(2012?石家庄模拟)科学家一直致力于“人工固氮”的方法研究.(1)合成氨的原理为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,该反应的能量变化如图所示.
①在反应体系中加入催化剂,反应速率增大,E2的变化是
减小
减小
(填“增大”、“减小”或“不变”).②将0.3mol N2和0.5mol H2充入体积不变的密闭容器中,在一定条件下达到平衡,测得容器内气体压强变为原来的
| 7 |
| 8 |
30%
30%
;欲提高该容器中H2的转化率,下列措施可行的是AD
AD
(填选项字母).A.向容器中按原比例再充入原料气 B.向容器中再充入一定量H2
C.改变反应的催化剂 D.液化生成物分离出氨
(2)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3和TiO2)表面与水发生反应:
2N2(g)+6H2O(1)?4NH3(g)+3O2(g)△H=+1530kJ/mol
又知:H2O(1)=H2O(g)△H=+44.0kJ/mol
则2N2(g)+6H2O(g)?4NH3(g)+3O2(g)△H=
+1266
+1266
kJ/mol,该反应的化学平衡常数表达式为K=| C4(NH3)C3(O2) |
| C2(N2)C6(H2O) |
| C4(NH3)C3(O2) |
| C2(N2)C6(H2O) |
不变
不变
(填“增大”、“减小”或“不变”).分析:(1)①根据催化剂降低反应的活化能;
②根据化学平衡的三部曲列式计算出氢气的转化率;根据影响化学平衡的条件分析判断以及增大一种物质的浓度会提高另一种物质的转化率;
(2)根据根据盖斯定律来分析;化学平衡常数是用平衡状态下生成物平衡浓度的幂次方乘积除以反应物的幂次方乘积;根据化学平衡常数的影响因素来判断.
②根据化学平衡的三部曲列式计算出氢气的转化率;根据影响化学平衡的条件分析判断以及增大一种物质的浓度会提高另一种物质的转化率;
(2)根据根据盖斯定律来分析;化学平衡常数是用平衡状态下生成物平衡浓度的幂次方乘积除以反应物的幂次方乘积;根据化学平衡常数的影响因素来判断.
解答:解:(1)①在反应体系中加入催化剂,反应速率增大,降低了反应的活化能,依据图示可知E2减小,故答案为:减小;
②N2(g)+3H2(g)?2NH3(g)
起始量(mol) 0.3 0.5 0
变化量(mol) x 3x 2x
平衡量(mol) 0.3-x 0.5-3x 2x
容器内气体压强变为原来的
,即气体的物质的量变为为原来的
,则
=
,x=0.05,
H2的转化率为
×100%=30%,A、向容器中按原比例再充入原料气,相当于增大容器内的压强,平衡正向进行,提高氢气的转化率,故A正确;
B、向容器中再充入一定量H2,提高了N2的转化率,而本身的转化率降低,故B错误;
C、改变反应的催化剂,不改变化学平衡,不能提高氢气转化率,故C错误;
D、液化生成物分离出氨,减少生成物,平衡正向进行,提高氢气转化率,故D正确;
故答案为:30%;AD;
(2)①2N2(g)+6H2O(1)?4NH3(g)+3O2(g)△H=+1530kJ/mol
②H2O(1)=H2O(g)△H=+44.0kJ/mol
由①-②×6得:2N2(g)+6H2O(g)?4NH3(g)+3O2(g)△H=+1266kJ/mol;
该反应的化学平衡常数表达式为K=
,
化学平衡常数的大小只与温度有关,故增大压强,K值不变,
故答案为:+1266;
;不变.
②N2(g)+3H2(g)?2NH3(g)
起始量(mol) 0.3 0.5 0
变化量(mol) x 3x 2x
平衡量(mol) 0.3-x 0.5-3x 2x
容器内气体压强变为原来的
| 7 |
| 8 |
| 7 |
| 8 |
| 0.3-x+0.5-3x+ 2x |
| 0.3+0.5 |
| 7 |
| 8 |
H2的转化率为
| 0.15mol |
| 0.5 mol |
B、向容器中再充入一定量H2,提高了N2的转化率,而本身的转化率降低,故B错误;
C、改变反应的催化剂,不改变化学平衡,不能提高氢气转化率,故C错误;
D、液化生成物分离出氨,减少生成物,平衡正向进行,提高氢气转化率,故D正确;
故答案为:30%;AD;
(2)①2N2(g)+6H2O(1)?4NH3(g)+3O2(g)△H=+1530kJ/mol
②H2O(1)=H2O(g)△H=+44.0kJ/mol
由①-②×6得:2N2(g)+6H2O(g)?4NH3(g)+3O2(g)△H=+1266kJ/mol;
该反应的化学平衡常数表达式为K=
| C4(NH3)C3(O2) |
| C2(N2)C6(H2O) |
化学平衡常数的大小只与温度有关,故增大压强,K值不变,
故答案为:+1266;
| C4(NH3)C3(O2) |
| C2(N2)C6(H2O) |
点评:本题考查了化学平衡的三部曲计算方法,影响平衡常数、化学反应速率、化学平衡的因素等应用,综合性较大,题目难度中等.

练习册系列答案
相关题目
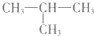 (2012?石家庄一模)2-甲基丙烷(如图)的二氯代物共有(不考虑立体异构)( )
(2012?石家庄一模)2-甲基丙烷(如图)的二氯代物共有(不考虑立体异构)( )