题目内容
【题目】一定温度下,在2L的密闭容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示
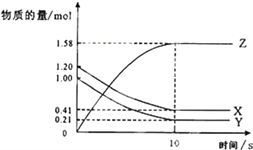
(1)该反应的化学方程式为____________________________________
(2)用Z表示的化学反应速率为_________________________
(3)在密闭容器中,下列条件的改变引起该反应的反应速率的变化是什么(填“加快”“不变”或“减慢”)。
A.缩小容器体积使压强增大:________。
B.体积不变充入Z气体使压强增大:________。
C.体积不变充入氩气使压强增大:________。
【答案】 X + Y ![]() 2Z 0.079 mol/(Ls) 加快 加快 不变
2Z 0.079 mol/(Ls) 加快 加快 不变
【解析】(1)由图像可以看出,随着反应的进行,X、Y的物质的量减少,Z的物质的量增加,所以X、Y是反应物,Z是生成物。在10s后三种物质的物质的量均为定值,不为0,所以反应是可逆反应。再根据图像得△n(X):△n(Y):△n(Z)= (1.20-0.41)mol:(1.00-0.21)mol:(1.58-0)mol=1:1:2,因参加反应的物质其物质的量之比等于化学计量数之比,所以化学方程式是X + Y ![]() 2Z 。
2Z 。
(2)根据化学反应速率的计算公式,用Z表示的化学反应速率为ν(Z)=![]() =0.079 mol/(Ls)。
=0.079 mol/(Ls)。
(3)A项,缩小体积使压强增大,各组分的浓度增大,反应速率加快,所以答案是:加快;B项体积不变充入Z气体,会使Z气体的浓度增大,反应速率加快,所以答案是:加快;C项,体积不变充入氩气使压强增大,因参加反应的各气体的浓度不变,则反应速率不变,故答案是:不变。

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目