��Ŀ����
����Ŀ���������ң���Ҫ�ɷ�ΪAl��Al2O3��AlN��FeO�ȣ��Ʊ�������[��Ҫ�ɷ�ΪAl��OH2Cl��]��һ�ֹ������£� 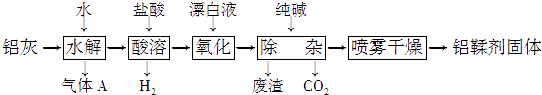
��1������A��ʹʪ��ĺ�ɫʯ����ֽ������������90��ˮ������A�Ļ�ѧ����ʽΪ����ˮ�⡱����90������������½��е�ԭ���� ��
��2�������ܡ�ʱ��Al2O3������Ӧ�����ӷ���Ϊ ��
��3����������ʱ��������Ӧ�����ӷ���ʽΪ ��
��4�����������ɷ�Ϊ���ѧʽ����
��5�������������������������ԭ���� ��
��6������������茶��壬��������Ҫ��Ӧ�ǣ�4[NH4Al��SO4��212H2O] ![]() 2Al2O3+2NH3��+N2��+5SO3��+3SO2��+53H2O��������������ͨ����ͼ��ʾ��װ�ã���
2Al2O3+2NH3��+N2��+5SO3��+3SO2��+53H2O��������������ͨ����ͼ��ʾ��װ�ã���
�ټ���ƿ���ռ��������������ѧʽ����
����������NaHSO3��Һ���յ����ʳ���H2O��g��������ѧʽ��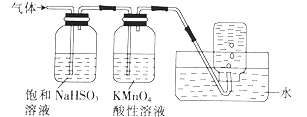
���𰸡�
��1��+3H2O ![]() ?Al��OH��3+NH3��������NH3��ˮ�е��ܽ�ȣ���ʹNH3�ݳ�
?Al��OH��3+NH3��������NH3��ˮ�е��ܽ�ȣ���ʹNH3�ݳ�
��2��Al2O3+6H+�T2Al3++3H2O
��3��2Fe2++2H++ClO���T2Fe3++Cl��+H2O
��4��Fe��OH��3
��5����ֹAl��OH��2Clˮ������Al��OH��3
��6��N2��NH3��SO3
���������⣺������Ҫ�ɷ�ΪAl��Al2O3��AlN��FeO�ȼ���ˮ������Ӧ��AlN��ˮ��Ӧ�������������Ͱ����������������ܺ������Ȼ�����Һ���Ȼ�������Һ������Ư��������������Ϊ�����ӣ����봿�������ҺPHʹ������ȫ���������������������Ʊ���������
��1.������A��ʹʪ��ĺ�ɫʯ����ֽ������˵�����ɵ��ǰ����������е�AlN��ˮ����ˮ�ⷴӦ�����������������Ͱ�������Ӧ�Ļ�ѧ����ʽΪ��AlN+3H2O ![]() Al��OH��3+NH3�������ȿ��Դٽ�������ˮ�����ɰ���������NH3��ˮ�е��ܽ�ȣ���ʹNH3�ݳ������Դ��ǣ�+3H2O
Al��OH��3+NH3�������ȿ��Դٽ�������ˮ�����ɰ���������NH3��ˮ�е��ܽ�ȣ���ʹNH3�ݳ������Դ��ǣ�+3H2O ![]() Al��OH��3+NH3��������NH3��ˮ�е��ܽ�ȣ���ʹNH3�ݳ���
Al��OH��3+NH3��������NH3��ˮ�е��ܽ�ȣ���ʹNH3�ݳ���
��2.������������������������ʱ�����ᷢ����Ӧ�����Ȼ�����Һ���������ܡ�ʱ��Al2O3������Ӧ�����ӷ���ʽΪ��Al2O3+6H+�T2Al3++3H2O�����Դ��ǣ�Al2O3+6H+�T2Al3++3H2O��
��3.������Ư��Һ�����������ô����������������Һ�е�ǿ������������������Ϊ�����ӣ���Ӧ�����ӷ���ʽΪ��2Fe2++2H++ClO���T2Fe3++Cl��+H2O�����Դ��ǣ�2Fe2++2H++ClO���T2Fe3++Cl��+H2O��
��4.������������֪���������ɷ�Ϊ����������������ѧʽΪ��Fe��OH��3 �� ���Դ��ǣ�Fe��OH��3��
��5.����������Ҫ�ɷ�ΪAl��OH��2Cl���ڼ�������ʱ�ᷢ��ˮ�⣬Ϊ��ֹˮ�����������������������ˮ�⣬���Դ��ǣ���ֹAl��OH��2Clˮ������Al��OH��3��
��6.�������������У��������������ƿ����հ���������������������ն�������������յ��������Դ��ǣ�N2����NH3��SO3�ܹ������������Ʒ�Ӧ��������������NaHSO3��Һ���յ����ʳ���H2O��g�����NH3��SO3 ��
���Դ��ǣ�NH3��SO3 ��