题目内容
【题目】常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液,有关粒子的物质的量变化如图所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-)。下列说法正确的是

A. M点溶液中:2c(HA-)+c(A2-)=0.2 mol/L
B. N点溶液呈酸性,则c(Na+) < 3c(HA-)
C. 若N点溶液pH =4.2,则Ka2(H2A)的数量级为104
D. V(NaOH)=20mL时,溶液中:c(H+) < c(OH-)
【答案】B
【解析】A. M点溶液体积大于20mL,2c(HA-)+c(A2-)<0.2 mol/L,故A错误;B. 溶液中电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HA-)+2c(A2-),N点溶液呈酸性,c(H+)>c(OH-),c(HA-)=c(A2-),则c(Na+) < 3c(HA-),故B正确;C. 若N点溶液pH =4.2,c(H+)=10-4.2mol/L,c(HA-)+2c(A2-),则Ka2(H2A)= 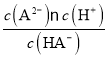 =c(H+)=10-4.2=10-(5-0.8),数量级为105,故C错误;D. N点溶液pH =4.2,所以V(NaOH)=20mL时的溶液中:c(H+) > c(OH-),故D错误。故选B。
=c(H+)=10-4.2=10-(5-0.8),数量级为105,故C错误;D. N点溶液pH =4.2,所以V(NaOH)=20mL时的溶液中:c(H+) > c(OH-),故D错误。故选B。

练习册系列答案
相关题目