题目内容
如图表示某温度时,反应N2O4(g) 2NO2(g)在前110 s内的反应进行情况,请根据图像回答下列问题。
2NO2(g)在前110 s内的反应进行情况,请根据图像回答下列问题。
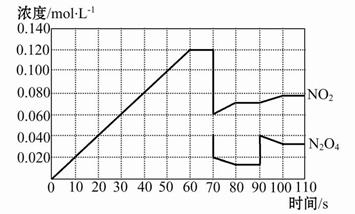
(1)该可逆反应达到平衡的时间段为 。
(2)反应进行到70 s时,改变的条件可能是 (填字母,下同),反应进行到90 s时,改变的条件可能是 。
(3)90 s后若维持容器的体积不变,平衡移动的方向为 (填“正反应”、“逆反应”或“不移动”),此时N2O4的转化率 (填“增大”、“减小”或“不变”)。
(4)请在图中画出反应物N2O4在0~70秒时的浓度变化曲线。
 2NO2(g)在前110 s内的反应进行情况,请根据图像回答下列问题。
2NO2(g)在前110 s内的反应进行情况,请根据图像回答下列问题。
(1)该可逆反应达到平衡的时间段为 。
(2)反应进行到70 s时,改变的条件可能是 (填字母,下同),反应进行到90 s时,改变的条件可能是 。
| A.加入催化剂 | B.扩大容器体积 |
| C.升高温度 | D.增大N2O4的浓度 |
(4)请在图中画出反应物N2O4在0~70秒时的浓度变化曲线。
(1)60~70 s、80~90 s、100~110 s (2)B D
(3)正反应 减小
(4)

(3)正反应 减小
(4)

(1)由图像可知反应达到平衡的时间段为60~70 s、80~90 s和100~110 s。
(2)反应进行到70 s时改变某一条件,可以看出NO2的浓度迅速从0.120 mol·L-1减小到0.060 mol·L-1,N2O4的浓度从0.040 mol·L-1减小到0.020 mol·L-1,两者的浓度都减小到原来的1/2,说明改变的条件为增大容器的体积为原来的2倍或减小压强为原来的1/2;90 s时突然改变某一条件可以看出NO2的浓度瞬间没有改变,但是N2O4的浓度瞬间增大,说明改变的条件是增大了N2O4的浓度。
(3)根据(2)可知,90 s后平衡向正反应方向移动;增大N2O4的浓度,在恒容容器中相当于增大压强,则N2O4的转化率减小。
(4)从图像可知,NO2为反应物,N2O4为生成物。60 s达到平衡时NO2的浓度增大了0.120 mol·L-1,说明N2O4反应过程中浓度减少了0.060 mol·L-1,因为已知在70 s时N2O4的浓度为0.040 mol·L-1,所以N2O4的起始浓度为0.040 mol·L-1+
0.060 mol·L-1="0.100" mol·L-1。
(2)反应进行到70 s时改变某一条件,可以看出NO2的浓度迅速从0.120 mol·L-1减小到0.060 mol·L-1,N2O4的浓度从0.040 mol·L-1减小到0.020 mol·L-1,两者的浓度都减小到原来的1/2,说明改变的条件为增大容器的体积为原来的2倍或减小压强为原来的1/2;90 s时突然改变某一条件可以看出NO2的浓度瞬间没有改变,但是N2O4的浓度瞬间增大,说明改变的条件是增大了N2O4的浓度。
(3)根据(2)可知,90 s后平衡向正反应方向移动;增大N2O4的浓度,在恒容容器中相当于增大压强,则N2O4的转化率减小。
(4)从图像可知,NO2为反应物,N2O4为生成物。60 s达到平衡时NO2的浓度增大了0.120 mol·L-1,说明N2O4反应过程中浓度减少了0.060 mol·L-1,因为已知在70 s时N2O4的浓度为0.040 mol·L-1,所以N2O4的起始浓度为0.040 mol·L-1+
0.060 mol·L-1="0.100" mol·L-1。

练习册系列答案
相关题目
 2SO3,正反应速率分别用v(SO2)、v(O2)、v(SO3)(mol·L-1·min-1)表示,逆反应速率分别用v′(SO2)、v′(O2)、v′(SO3)(mol·L-1·min-1)表示,当反应达到化学平衡时,正确的关系是
2SO3,正反应速率分别用v(SO2)、v(O2)、v(SO3)(mol·L-1·min-1)表示,逆反应速率分别用v′(SO2)、v′(O2)、v′(SO3)(mol·L-1·min-1)表示,当反应达到化学平衡时,正确的关系是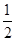 v′(SO2)
v′(SO2)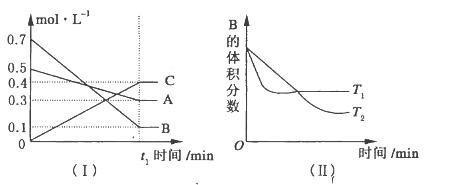
 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
 p C(g)+q D(g)的反应中,经5 min达到平衡,测得A增加3 mol·L-1,B增加1 mol·L-1,C减少2 mol·L-1,此时若给体系加压,平衡不移动,则m∶n∶p∶q为( )
p C(g)+q D(g)的反应中,经5 min达到平衡,测得A增加3 mol·L-1,B增加1 mol·L-1,C减少2 mol·L-1,此时若给体系加压,平衡不移动,则m∶n∶p∶q为( ) 2NH3(g)+CO2(g)
2NH3(g)+CO2(g) O2(g)
O2(g) CO(g)+2H2(g) ΔH<0
CO(g)+2H2(g) ΔH<0