题目内容
(12分)海水资源的利用具有广阔前景。海水中主要离子的含量如下:
(1)电渗析法淡化海水示意图如图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过。
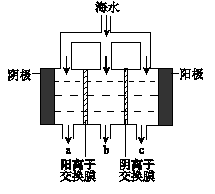
①阳极主要电极反应式是 。
②在阴极附近产生少量白色沉淀,其成分有 和CaCO3,生成CaCO3的离子方程式是 。
③淡水的出口为 (填“a”、“b”或“c”)。
(2)利用海水可以提取溴和镁,提取过程如下:
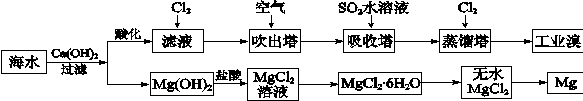
①提取溴的过程中,经过2次Br-→Br2转化的目的是 ,吸收塔中发生反应的离
子方程式是 。用平衡移动原理解释通空气的目的是 。
②从MgCl2溶液中得到MgCl2·6H2O晶体的主要操作是 、过滤、洗涤、干燥。
③依据上述流程,若将10 m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为 L(忽略Cl2溶解)。
| 成分 | 含量/(mg L-1) | 成分 | 含量/(mg L-1) |
| Cl- | 18980 | Ca2+ | 400 |
| Na+ | 10560 | HCO3- | 142 |
| SO42- | 2560 | Br- | 64 |
| Mg2+ | 1272 | | |

①阳极主要电极反应式是 。
②在阴极附近产生少量白色沉淀,其成分有 和CaCO3,生成CaCO3的离子方程式是 。
③淡水的出口为 (填“a”、“b”或“c”)。
(2)利用海水可以提取溴和镁,提取过程如下:

①提取溴的过程中,经过2次Br-→Br2转化的目的是 ,吸收塔中发生反应的离
子方程式是 。用平衡移动原理解释通空气的目的是 。
②从MgCl2溶液中得到MgCl2·6H2O晶体的主要操作是 、过滤、洗涤、干燥。
③依据上述流程,若将10 m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为 L(忽略Cl2溶解)。
(12分)
(1)①(1分)2Cl—-2e—=Cl2↑
②(1分)Mg(OH)2 (2分)Ca2++ OH—+HCO3—=CaCO3↓+H2O
③(1分)b
(2)①(1分)对溴元素进行富集 (2分)SO2+Br2+2H2O=4H++2Br—+SO42—
(1分)通入空气将Br2蒸气带出,使Br2(g) Br2(aq)或
Br2(aq)或
Br2+H2O HBr+HBrO平衡向左移动
HBr+HBrO平衡向左移动
②(1分)加热浓缩、冷却结晶
③(2分)182
(1)①(1分)2Cl—-2e—=Cl2↑
②(1分)Mg(OH)2 (2分)Ca2++ OH—+HCO3—=CaCO3↓+H2O
③(1分)b
(2)①(1分)对溴元素进行富集 (2分)SO2+Br2+2H2O=4H++2Br—+SO42—
(1分)通入空气将Br2蒸气带出,使Br2(g)
 Br2(aq)或
Br2(aq)或Br2+H2O
 HBr+HBrO平衡向左移动
HBr+HBrO平衡向左移动②(1分)加热浓缩、冷却结晶
③(2分)182
(1)在阳极放电的离子为阴离子,且阴离子的放电能力由强到弱的顺序为:S2->I->Br->CL->OH->含氧酸根离子>F-,所以该阳极的电极反应式为CL-放电。
在阴极放电的离子为阳离子,且阳离子的放电能力由强到的顺序为:Ag+>Fe3+>Cu2+>H+(酸)>Pb2+>Sn2+>Fe2+>Zn2+>H+(水)>AL3+>Mg2+>Na+>Ca2+>K+;所以该阴极的电极反应式为H+(水)放电,破坏了水的电离平衡,使阴极附近OH-浓度增大;
(2)在滤液中通入CL2是将滤液中的Br-氧化为Br2,再利用热的空气将Br2吹出,进入吸收塔与SO2反应,其反应的离子方程式为:SO2+Br2+2H2O=4H++2Br—+SO42—;再通入CL2将Br-氧化为Br2,两次Br-→Br2转化的目的是对溴元素进行富集;
在阴极放电的离子为阳离子,且阳离子的放电能力由强到的顺序为:Ag+>Fe3+>Cu2+>H+(酸)>Pb2+>Sn2+>Fe2+>Zn2+>H+(水)>AL3+>Mg2+>Na+>Ca2+>K+;所以该阴极的电极反应式为H+(水)放电,破坏了水的电离平衡,使阴极附近OH-浓度增大;
(2)在滤液中通入CL2是将滤液中的Br-氧化为Br2,再利用热的空气将Br2吹出,进入吸收塔与SO2反应,其反应的离子方程式为:SO2+Br2+2H2O=4H++2Br—+SO42—;再通入CL2将Br-氧化为Br2,两次Br-→Br2转化的目的是对溴元素进行富集;

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
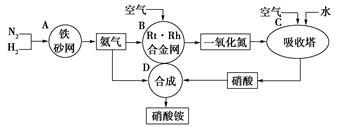
 (1)吸收塔C中通人空气的目的是
(1)吸收塔C中通人空气的目的是  2NH3(g);△H=-92kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)
2NH3(g);△H=-92kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)

 2H2O
2H2O