题目内容
(1)AgNO3的水溶液呈酸性的原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,充分反应后溶液呈中性,则反应后溶液存在的离子有 ,其浓度由大到小的顺序为 ,氨水的浓度a 0.01 mol·L-1(填“>”、“<”或“=”)。
(3)用已知浓度的NaOH标准溶液滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是
(2)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,充分反应后溶液呈中性,则反应后溶液存在的离子有 ,其浓度由大到小的顺序为 ,氨水的浓度a 0.01 mol·L-1(填“>”、“<”或“=”)。
(3)用已知浓度的NaOH标准溶液滴定未知浓度的盐酸,选用酚酞为指示剂,造成测定结果偏高的原因可能是
| A.未用标准液润洗碱式滴定管; |
| B.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液; |
| C.盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗; |
| D.滴定终点读数时,俯视滴定管的刻度,其它操作均正确; |
⑴Ag++ H2O 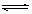 AgOH +H+ 抑制
AgOH +H+ 抑制
⑵OH-、H+、NH4+、Cl- c(Cl-)=c(NH4+)>c(H+)=c(OH-) >
⑶AB
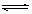 AgOH +H+ 抑制
AgOH +H+ 抑制⑵OH-、H+、NH4+、Cl- c(Cl-)=c(NH4+)>c(H+)=c(OH-) >
⑶AB
试题分析:(1)银离子在水溶液中可发生水解,有氢离子生成,所以溶液显酸性。硝酸中会存在大量的氢离子,所以可以抑制硝酸银的水解(2)产物是氯化铵和水,所以溶液中会存在氢氧根离子、氢离子、铵根离子、氯离子。主要产物是氯化铵,而铵根离子会发生水解生成氢氧根离子,而从题意可知溶液呈中性,所以排序为
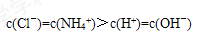

练习册系列答案
相关题目
 )
) )>c(H2CO3)
)>c(H2CO3) 2CO2+N2△H<0,则该反应一定能自发进行
2CO2+N2△H<0,则该反应一定能自发进行