题目内容
A和B均为钠盐的水溶液,A呈中性,B呈碱性并具有氧化性.下述为相关实验步骤和实验现象:
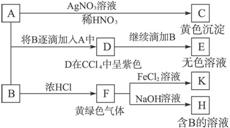
请回答:
(1)写出A、B和C的化学式:A
(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
(3)写出将SO2气体通入K溶液中发生反应的离子方程式:
(4)写出由F→H的化学方程式:

请回答:
(1)写出A、B和C的化学式:A
NaI
NaI
,BNaClO
NaClO
,CAgI
AgI
;(2)依次写出A→D和D→E(E中含有某+5价元素的含氧酸根离子)的离子方程式:
2I-+ClO-+H2O=I2+Cl-+2OH-
2I-+ClO-+H2O=I2+Cl-+2OH-
,I2+5ClO-+2OH-=2IO3-+5Cl-+H2O
I2+5ClO-+2OH-=2IO3-+5Cl-+H2O
;(3)写出将SO2气体通入K溶液中发生反应的离子方程式:
2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
;(4)写出由F→H的化学方程式:
Cl2+2NaOH=NaClO+NaCl+H2O
Cl2+2NaOH=NaClO+NaCl+H2O
.分析:钠盐A能和AgNO3溶液反应生成一种难溶于HNO3的黄色沉淀,可确定A为NaI,C为AgI;黄绿色气体F是Cl2;F和NaOH溶液反应生成钠盐B,根据B呈碱性并具有氧化性,可知B为NaClO(NaCl、NaClO3溶液均呈中性);NaClO具有强氧化性,能氧化NaI,少量NaClO将NaI氧化成I2,进一步反应生成NaIO3,其中I为+5价;Cl2氧化FeCl2生成FeCl3,FeCl3又能氧化SO2生成SO42-.
解答:解:钠盐A能和AgNO3溶液反应生成一种难溶于HNO3的黄色沉淀,可确定A为NaI,C为AgI;黄绿色气体F是Cl2;F和NaOH溶液反应生成钠盐B,根据B呈碱性并具有氧化性,可知B为NaClO(NaCl、NaClO3溶液均呈中性);NaClO具有强氧化性,能氧化NaI,少量NaClO将NaI氧化成I2,进一步反应生成NaIO3,其中I为+5价;Cl2氧化FeCl2生成FeCl3,FeCl3又能氧化SO2生成SO42-,则
(1)由以上分析可知A为NaI,B为NaClO,C为AgI,故答案为:NaI; NaClO; AgI;
(2)NaClO具有强氧化性,能氧化NaI,少量NaClO将NaI氧化成I2,反应的离子方程式为2I-+ClO-+H2O=I2+Cl-+2OH-,
进一步反应可把I2氧化为NaIO3,反应的离子方程式为I2+5ClO-+2OH-=2IO3-+5Cl-+H2O,
故答案为:2I-+ClO-+H2O=I2+Cl-+2OH-; I2+5ClO-+2OH-=2IO3-+5Cl-+H2O;
(3)FeCl3能氧化SO2生成SO42-,反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,
故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
(4)F→H为Cl2与NaOH的反应,反应的方程式为Cl2+2NaOH=NaClO+NaCl+H2O,故答案为:Cl2+2NaOH=NaClO+NaCl+H2O.
(1)由以上分析可知A为NaI,B为NaClO,C为AgI,故答案为:NaI; NaClO; AgI;
(2)NaClO具有强氧化性,能氧化NaI,少量NaClO将NaI氧化成I2,反应的离子方程式为2I-+ClO-+H2O=I2+Cl-+2OH-,
进一步反应可把I2氧化为NaIO3,反应的离子方程式为I2+5ClO-+2OH-=2IO3-+5Cl-+H2O,
故答案为:2I-+ClO-+H2O=I2+Cl-+2OH-; I2+5ClO-+2OH-=2IO3-+5Cl-+H2O;
(3)FeCl3能氧化SO2生成SO42-,反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,
故答案为:2Fe3++SO2+2H2O=2Fe2++SO42-+4H+;
(4)F→H为Cl2与NaOH的反应,反应的方程式为Cl2+2NaOH=NaClO+NaCl+H2O,故答案为:Cl2+2NaOH=NaClO+NaCl+H2O.
点评:本题考查无机物的推断,题目难度中等,此题解题突破口为几种物质的颜色,由此可知为卤素单质及其化合物之间的相互转变,答题时注意体会.

练习册系列答案
相关题目

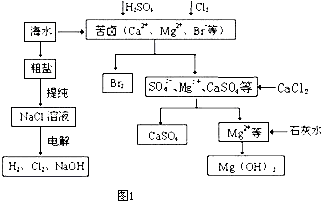
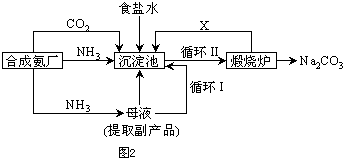
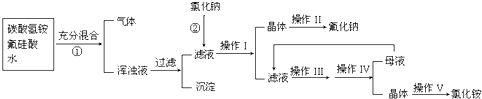
 等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是_________(填序号);
等杂质,必须精制后才能供电解使用。精制时,粗盐溶于水过滤后,还要加入的试剂分别为①Na2CO3、②HCl(盐酸)、③BaCl2,这3种试剂添加的合理顺序是_________(填序号);
