题目内容
(12分)市场上出售的“热敷袋”其主要成分是铁屑、炭粉和少量的NaCl、水等。热敷袋在启用前用塑料袋使之与空气隔绝,启用时,打开塑料袋轻轻揉搓,就会放出热量,使用完后,会发现袋内有许多铁锈生成。回答:
(1)热敷袋放出的热量来源于_________放出的热量。
(2)炭粉的作用是________________________。
(3)加入NaCl的作用是________________________。
(4)写出有关电极反应式和化学方程式________________。
(1)热敷袋放出的热量来源于_________放出的热量。
(2)炭粉的作用是________________________。
(3)加入NaCl的作用是________________________。
(4)写出有关电极反应式和化学方程式________________。
( 12 分)(1)铁屑被氧化 (2)C、Fe与NaCl、水组成原电池,C作正极,使铁氧化速率加快 (3)溶于水形成电解质溶液,增强导电性 (4)正极反应:O2+2H2O+4e-====4OH-,负极反应:2Fe-4e-====2Fe2+,发生的反应有
Fe2++2OH-==Fe(OH)2↓,
4Fe(OH)2+O2+2H2O====4Fe(OH)3,
2Fe(OH)3====Fe2O3·xH2O+(3-x)H2O
Fe2++2OH-==Fe(OH)2↓,
4Fe(OH)2+O2+2H2O====4Fe(OH)3,
2Fe(OH)3====Fe2O3·xH2O+(3-x)H2O
略

练习册系列答案
 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目

 ClO(g)+3H2(g)△H>0。
ClO(g)+3H2(g)△H>0。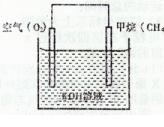
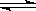 2SO3(g);ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是
2SO3(g);ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是