题目内容
【题目】向绝热恒容密闭容器中通入![]() 和
和![]() ,在一定条件下使反应
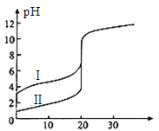
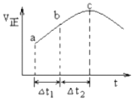
,在一定条件下使反应![]() 达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
达到平衡,正反应速率随时间变化的示意图如图所示。由图可得出的正确结论是
A.在c点容器内气体颜色不再改变
B.生成物的总能量高于反应物的总能量
C.![]() 时,
时,![]() 的转化率:
的转化率:![]() 段小于
段小于![]() 段
段
D.在恒温恒容密闭容器中通入相同的![]() 和
和![]() ,反应物平衡转化率小于绝热恒容容器
,反应物平衡转化率小于绝热恒容容器
【答案】C
【解析】
反应开始时,反应物浓度最大,则正反应速率应该最大,随着反应的进行,正反应速率应该减小,但图象中正反应速率却逐渐增大,说明反应为放热反应,温度升高,当反应进行到一定阶段时,由于反应物浓度逐渐减小,则反应速率逐渐减小,据此分析解答。
![]() 当正反应速率不变时,达到化学平衡状态,但c点反应速率最大,虽然正反应速率减小,但反应继续向正反应方向进行,没有达到平衡状态,所以c点容器内气体颜色变浅,故A错误;
当正反应速率不变时,达到化学平衡状态,但c点反应速率最大,虽然正反应速率减小,但反应继续向正反应方向进行,没有达到平衡状态,所以c点容器内气体颜色变浅,故A错误;
B. 该反应正向放热,所以反应物总能量大于生成物总能量,故B错误;
C. a点到b点,b点到c点反应均未达到平衡,随着反应的进行,体系温度升高,反应速率加快,![]() 的转化率增大,所以
的转化率增大,所以![]() 的转化率:
的转化率:![]() 段小于
段小于![]() 段,故C正确;
段,故C正确;
D. 反应正向放热,绝热恒容密闭容器中温度升高,恒温恒容密闭容器中通入相同的![]() 和
和![]() 的反应体系相当在绝热恒容体系中降温,平衡正向进行,反应物平衡转化率增大,所以恒温恒容密闭容器中通入相同的
的反应体系相当在绝热恒容体系中降温,平衡正向进行,反应物平衡转化率增大,所以恒温恒容密闭容器中通入相同的![]() 和
和![]() ,反应物平衡转化率大于绝热恒容容器,故D错误;
,反应物平衡转化率大于绝热恒容容器,故D错误;
故选C。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案【题目】用Na2FeO4溶液氧化废水中的还原性污染物M,为研究降解效果,设计如下对比实验探究温度、浓度、 pH、催化剂对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示,下列说法不正确的是( )

实验编号 | 温度℃ | pH |
① | 25 | 1 |
② | 45 | 1 |
③ | 25 | 7 |
④ | 25 | 1 |
A.实验①在15 min内M的降解速率为1.33×10-5mol/(L·min)
B.若其他条件相同,实验①②说明升高温度,M降解速率增大
C.若其他条件相同,实验①③证明pH越高,越不利于M的降解
D.实验④说明M的浓度越小,降解的速率越快