题目内容
【题目】实验室利用如图装置进行中和热的测定.回答下列问题: 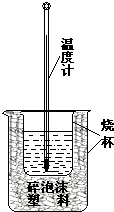
(1)如图装置中,为了酸碱能更充分地反应,应该增加一个(填玻璃仪器名称);大烧杯上没有盖上硬纸板,测得的中和热数值将会(填“偏大”、“偏小”或“无影响”).
(2)在操作正确的前提下提高中和热测定的准确性的关键是( 填代号)
A.进行实验时的气温
B.装置的保温隔热效果
C.实验所用酸碱溶液的体积
(3)如果用0.5 mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”的数值将(填“偏大”、“偏小”、“不变”);原因是
【答案】
(1)环形搅拌器(或环形玻璃棒);偏小
(2)B
(3)偏大;固体NaOH溶于水放热
【解析】解:①中和热的测定时,为了加快反应速率、使反应充分进行,应用环形玻璃搅拌棒来搅拌;如果没有盖硬纸板,会导致热量的损失,则导致所测得的中和热的数值偏小,所以答案是:环形搅拌器(或环形玻璃棒);偏小;②在中和反应中,必须确保热量不散失,故操作过程中的保温隔热是关键,故选B;③氢氧化钠固体溶于水放热,所以实验中测得的“中和热”数值将偏大,所以答案是:偏大;氢氧化钠固体溶于水放热.

【题目】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4 -+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。某实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计方案如下(KMnO4溶液已酸化):
实验序号 | A溶液 | B溶液 |
① | 20mL 0.lmol·L-l H2C2O4溶液 | 30mL 0.01mol.L-l KMnO4溶液 |
② | 20mL 0.2mol·L-l H2C2O4溶液 | 30mL 0.01mol.L-l KMnO4溶液 |

(1)该实验探究的是______对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是_____(填实验序号)。
(2)若实验①在2min末注射器的活塞向右移动到了b mL的位置,则这段时间的反应速率可表示为v(CO2)=______mL/min。若实验②在t min收集了4.48×10-3L CO2(标准状况下),则t min末c(MnO4-)=______。
(3)该小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是:①___________、②___________。
(4)已知草酸是一种二元弱酸,其电离常数K1=5.4×10-2、K2=5.4×10-5,写出草酸的电离方程式_______、________。试从电离平衡移动的角度解释K1>>K2的原因_______________。
【题目】如表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ |
(1)在这些元素中,化学性质最不活泼的是:(填具体元素符号,下同).
(2)NH3电子式是:;
(3)④、⑤、⑥的原子半径由大到小的顺序为 . (用元素符号表示)
(4)①、⑥、⑦的最高价氧化物对应水化物的酸性最强的是 . (用化学式表示)
(5)写出 ⑥的原子结构示意图;
(6)③氢化物的沸点(填“大于”、“小于”)⑥的氢化物的沸点.
