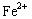题目内容
如图,水槽中试管内有一枚铁钉,放置数天观察:
(1)若液面上升,则溶液呈______性,电极反应式为:
负极:______,
正极:______
(2)若液面下降,则溶液呈______性,电极反应式为:
负极:______,
正极:______.

(1)若液面上升,则溶液呈______性,电极反应式为:
负极:______,
正极:______
(2)若液面下降,则溶液呈______性,电极反应式为:
负极:______,
正极:______.

生铁中含有碳,铁、碳和合适的电解质溶液构成原电池,
(1)若试管内液面上升,说明电解质环境是碱性或是中性,试管内气体因和水反应而使其压强减小,发生的是吸氧腐蚀,铁作负极,负极上铁失电子发生氧化反应,电极反应式为:Fe-2e-═Fe2+,正极上氧气得电子发生还原反应,电极反应式为2H2O+O2+4e-═4OH-,
故答案为:碱性或是中性;2Fe-4e-=2Fe2+;2H2O+O2+4e-═4OH-;
(2)若试管内液面下降,说明金属的腐蚀中生成气体导致压强增大,则金属发生的是析氢腐蚀,溶液呈酸性,负极上铁失电子发生氧化反应,电极反应式为:Fe-2e-═Fe2+,正极上氢离子得电子发生还原反应,电极反应式为:4H++4e-═2H2↑,
故答案为:较强的酸;Fe-2e-═Fe2+;2H++2e-=H2↑.
(1)若试管内液面上升,说明电解质环境是碱性或是中性,试管内气体因和水反应而使其压强减小,发生的是吸氧腐蚀,铁作负极,负极上铁失电子发生氧化反应,电极反应式为:Fe-2e-═Fe2+,正极上氧气得电子发生还原反应,电极反应式为2H2O+O2+4e-═4OH-,
故答案为:碱性或是中性;2Fe-4e-=2Fe2+;2H2O+O2+4e-═4OH-;
(2)若试管内液面下降,说明金属的腐蚀中生成气体导致压强增大,则金属发生的是析氢腐蚀,溶液呈酸性,负极上铁失电子发生氧化反应,电极反应式为:Fe-2e-═Fe2+,正极上氢离子得电子发生还原反应,电极反应式为:4H++4e-═2H2↑,
故答案为:较强的酸;Fe-2e-═Fe2+;2H++2e-=H2↑.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
 ="="
="="