��Ŀ����
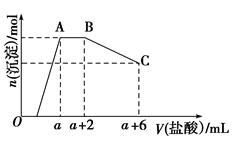
��֪X��M������ѧ�̲ij���Ԫ�أ����жԼס����������ӷ�Ӧͨʽ���ƶ��У����ף�XO3n��+Xn��+H����X����+H2O��δ��ƽ�������ң�Mm��+mOH����M(OH)m����������ȷ���ǣ� ��
����n=1����XO3n����XԪ��Ϊ+5�ۣ�Xλ�����ڱ��ڢ�A��
����m=1����M(NO3)m��Һ�Ͱ�ˮ����ʱ��������ܲ�ͬ
����m=2�����ڿ���������MSO4��Һ������һ���ܵõ�MSO4
����n=2����X����������ˮ��������������⻯�ﷴӦ
����m=3����MCl3�������ļ���Һ��Ӧһ������M(OH)m
����n=2��m=3����Xn����Mm�������ķ�Ӧ��ˮ�ⷴӦ
����n=1����XO3n����XԪ��Ϊ+5�ۣ�Xλ�����ڱ��ڢ�A��
����m=1����M(NO3)m��Һ�Ͱ�ˮ����ʱ��������ܲ�ͬ
����m=2�����ڿ���������MSO4��Һ������һ���ܵõ�MSO4
����n=2����X����������ˮ��������������⻯�ﷴӦ
����m=3����MCl3�������ļ���Һ��Ӧһ������M(OH)m
����n=2��m=3����Xn����Mm�������ķ�Ӧ��ˮ�ⷴӦ
| A���٢� | B���ڢ� | C���٢ڢۢ� | D��������� |
B
�������������n=1����X����ͼ�Ϊ-1�ۣ�XӦλ�����ڱ��ĵ�VIIA�壬������m=1�� +1���������У�Ag+��Na+��K+�ȣ�ֻ������������������ˮ�ij�����Ag++OH-=AgOH���������������ڰ�ˮ����������Һ���백ˮ������������Һ������������ˮ������������Һ�� ���������������μӳ����ܽ⣬����˳��ͬ����ͬ����ȷ����m=2����MΪFe������������+2�����ڿ������ױ�����Ϊ+3�ۣ�����������Һ�����ɡ����ղ����ܴﵽ��������������n=2��XԪ���γ�X2-���ӣ�X��ͼ�Ϊ-2�� Xֻ��Ϊ��������⣬Ũ���Ậ��ǿ�����ԣ������������⣬��ȷ����m=3������������ֻ�������������������Ȼ��������������Ʒ�Ӧ����û�����������������ɣ�������n=2��m=3��Xn-��Mm+���Էֱ���S2-��Fe3+�����߷���������ԭ��Ӧ���������Դ�ѡB��

��ϰ��ϵ�д�
�����Ŀ
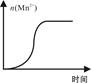
 ����Mn2����
����Mn2����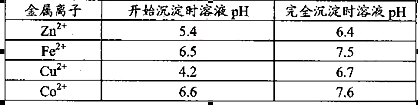
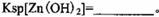 ��
��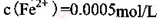 ������1
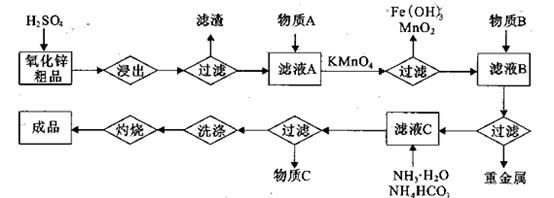
������1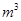 ����Һ��Fe2�������ĵ�KMnO4������Ϊ________g��������λ��Ч���֣���
����Һ��Fe2�������ĵ�KMnO4������Ϊ________g��������λ��Ч���֣���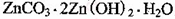 �����ɸó����Ļ�ѧ����ʽΪ________��
�����ɸó����Ļ�ѧ����ʽΪ________��