题目内容
在下列给定条件的溶液中,一定能大量共存的离子组是
| A.澄清透明溶液:H+、Na+、SO42-、C6H5O- |
| B.常温下Kw/c(H+)=0.1 mol/L的溶液:K+、Na+、SiO32-、NO3- |
| C.铁片加入产生气泡的溶液:Na+、NH4+、I-、NO2- |
| D.NaHCO3溶液:K+、Na+、SO42-、Al3+ |
B
试题分析:A. H++C6H5O-= C6H5OH↓.不能大量共存。错误。B.常温下Kw/c(H+)=0.1 mol/L的溶液,即Kw/c(H+)=C(OH-)="0.1" mol/L,溶液呈碱性,在该溶液中K+、Na+、SiO32-、NO3-不会发生任何离子反应,可以大量共存。正确。C.铁片加入产生气泡的溶液,说明溶液中含有大量的H+,溶液显酸性,此时会发生反应:H++NO2-= HNO2,HNO2有强的氧化性,能与I-发生氧化还原反应而不能大量共存。错误。D.在NaHCO3溶液中会发生离子反应:3HCO3-+Al3+=Al(OH)3↓+3CO2↑,不能大量共存。错误。

练习册系列答案
相关题目
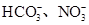 。已知该溶液可与Al2O3反应,则:
。已知该溶液可与Al2O3反应,则: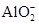 生成,则原溶液中一定含有_______,可能含有大量的_______。
生成,则原溶液中一定含有_______,可能含有大量的_______。