题目内容
下列各组物质的性质比较,正确的是( )
| A、稳定性:H2O<NH3<PH3<SiH4 |
| B、熔点:CO2<H2O<SiO2<KCl |
| C、酸性:HClO4>H3PO4>H2SO4>H2SiO3 |
| D、粒子半径:K+>Na+>Mg2+>Al3+ |
考点:非金属在元素周期表中的位置及其性质递变的规律,微粒半径大小的比较
专题:元素周期律与元素周期表专题
分析:A.非金属性越强对应的氢化物的稳定性越强;
B.熔点的一般规律为:原子晶体>离子晶体>分子晶体,结合氢键判断;
C.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
D.核外电子排布相同的离子,核电荷数越大,离子半径越小,核外电子层数越多,离子半径越大.
B.熔点的一般规律为:原子晶体>离子晶体>分子晶体,结合氢键判断;
C.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
D.核外电子排布相同的离子,核电荷数越大,离子半径越小,核外电子层数越多,离子半径越大.
解答:
解:A.非金属性O>N>P>Si,非金属性越强对应的氢化物的稳定性越强,故A错误;
B.SiO2为原子晶体,熔点最高,水中含有氢键,熔点顺序为CO2<H2O<KCl<SiO2,故B错误;
C.非金属性Cl>S>P>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故C错误;
D.K+>核外有3个电子层,离子半径最大,Na+、Mg2+、Al3+核外电子排布相同,核电荷数越大,离子半径越小,则粒子半径:K+>Na+>Mg2+>Al3+,故D正确.
故选D.
B.SiO2为原子晶体,熔点最高,水中含有氢键,熔点顺序为CO2<H2O<KCl<SiO2,故B错误;
C.非金属性Cl>S>P>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故C错误;
D.K+>核外有3个电子层,离子半径最大,Na+、Mg2+、Al3+核外电子排布相同,核电荷数越大,离子半径越小,则粒子半径:K+>Na+>Mg2+>Al3+,故D正确.
故选D.
点评:本题综合考查元素周期律知识,侧重于学生的分析能力的考查,注意把握比较问题的角度,学习中注意积累,难度中等.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
四个试管中都装有5mL 0.1mol?L-1 Na2S2O3溶液,分别在不同温度下加入下列硫酸,最先出现浑浊的是( )
| A、20℃,5mL,0.1 mol?L-1的硫酸 |
| B、20℃,4 mL,0.2 mol?L-1的硫酸 |
| C、30℃,3 mL,0.2 mol?L-1的硫酸 |
| D、30℃,4 mL,0.1 mol?L-1的硫酸 |
在一定温度下的定容密闭容器中,下列情况能表明可逆反应:H2(g)+I2(g)?2HI(g)已达平衡的是( )
| A、H2的生成速率与I2的生成速率相等 |
| B、反应容器内的压强不随时间的变化而变化 |
| C、H2、I2、HI的浓度相等 |
| D、若单位时间内生成n mol H2的同时生成2n mol HI |
关节炎是因为在关节滑液中形成了尿酸钠晶体,尤其是在寒冷季节易诱发关节疼痛,其化学机理如下:
①
②Ur-(aq)+Na+(aq)?NaUr(s).下列叙述正确的是( )
①

②Ur-(aq)+Na+(aq)?NaUr(s).下列叙述正确的是( )
| A、反应②的正反应为吸热反应 |
| B、增加Na+浓度,反应②平衡向逆反应方向移动 |
| C、反应②正反应为放热反应 |
| D、改变Na+浓度,对反应①平衡无影响 |
下列说法中正确的是( )
| A、向沸水中滴加饱和FeCl3溶液有红褐色沉淀产生 |
| B、制备AlCl3、CuCl2均可以采用将溶液直接蒸干的方法 |
| C、Ksp数值越大的难溶电解质在水中的溶解能力不一定越强 |
| D、向碳酸钡沉淀中加入稀硫酸,沉淀发生转化,可推知硫酸钡的Ksp比碳酸钡的大 |
原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,X、Z的最外层电子数之和与Y、W的最外层电子数之和相等.甲的化学式为YX3,是一种刺激性气味的气体,乙的化学式为YZ3,丙是由X、Y、Z组成的盐.下列说法正确的是( )
| A、原子半径:W>Y>Z,而离子半径:Z>Y>W |
| B、X的单质分子中存在s-pσ键 |
| C、测得丙的水溶液呈酸性,则溶液中丙盐阳离子浓度大于酸根离子浓度 |
| D、Y的单质分子中有一个p-pσ键和二个p-pπ键 |
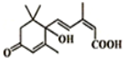 2012年广州市大街小巷对大量盆栽鲜花施用了诱抗素剂,以保证鲜花盛开,诱抗素的分子结构如图,下列关于该分子说法正确的是( )
2012年广州市大街小巷对大量盆栽鲜花施用了诱抗素剂,以保证鲜花盛开,诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A、诱抗素含有碳碳双键、羟基、羰基、羧基 |
| B、诱抗素能与氯化铁溶液发生显色反应 |
| C、诱抗素能发生加成反应、水解反应、氧化反应 |
| D、1mol诱抗素在一定条件下可分别与4mol H2、2mol NaOH发生反应 |
下列说法错误的是( )
A、
| ||||
B、
| ||||
| C、14C和14N的质量数相等,它们的中子数不等 | ||||
| D、12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同 |
下列分子式对应的结构式,从价键的成键情况看不合理的是( )
A、CH3N: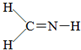 |
B、CH4Si: |
C、CH4S: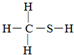 |
D、CH2SeO: |