题目内容
【题目】工业上以侯氏制碱法为基础生产焦亚硫酸钠(Na2S2O5).其制备工艺流程如下:

已知:反应Ⅱ包含2NaHSO3 Na2S2O5+H2O等多步反应.
(1)反应I的化学方程式为:_____________________________________________________ .
(2)已知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为:__________________________.
(3)反应I时应先通的气体为______,副产品X的化学式是______.
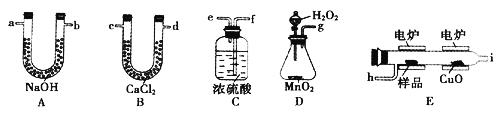
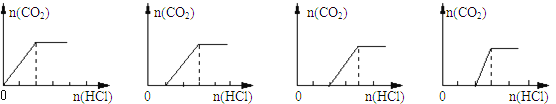
(4)为了减少产品Na2S2O5中杂质含量,需控制反应Ⅱ中气体与固体的物质的量之比约为______.检验产品中含有碳酸钠杂质所需试剂是______(填编号)
①酸性高锰酸钾②品红溶液③澄清石灰水
④饱和碳酸氢钠溶液⑤NaOH⑥稀硫酸.
【答案】 NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl S2O52-+2H+=2SO2↑+H2O NH3 CuSO45H2O 2:1 ①③⑥
【解析】反应Ⅰ为生成NaHCO3,加热生成Na2CO3,在反应Ⅱ中二氧化硫与碳酸钠反应生成NaHSO3与二氧化碳,加热NaHSO3生成Na2S2O5。硫化铜在空气中灼烧生成氧化铜和二氧化硫,氧化铜与稀硫酸反应生成硫酸铜,据此解答。
(1)根据流程可确定反应物为NaCl、NH3、CO2,产物为NH4Cl和碳酸氢钠,因此反应Ⅰ的化学方程式为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;
(2)根椐提示可知生成二氧化硫和水,Na2S2O5与稀硫酸反应放出SO2和水,反应的离子方程式为S2O52-+2H+=2SO2↑+H2O;
(3)由于二氧化碳在水中的溶解性很小,氨气极易溶于水,反应Ⅰ进行时应先通入氨气,增大HCO3-的浓度,便于NaHCO3析出;根据上述分析可知,氧化铜与硫酸反应生成硫酸铜,蒸发浓缩,冷却结晶,过滤洗涤,得出硫酸铜晶体,因此副产品X的化学式是CuSO45H2O;
(4)从图示中可以看出反应Ⅱ中气体与固体分别是二氧化硫和碳酸钠,这两种物质反应必须生成亚硫酸氢钠:反应Ⅱ中反应应是二氧化硫与碳酸钠反应生成NaHSO3,NaHSO3再生成Na2S2O5,反应方程式为Na2CO3+2SO2+H2O=2NaHSO3+CO2,因此气体与固体的物质的量之比为2:1;检验产品中含有碳酸钠杂质,需加酸反应检验二氧化碳生成,即用澄清石灰水,但加酸会生成二氧化硫,二氧化硫也能使澄清石灰水变浑浊,故应先除去,用酸性高锰酸钾溶液根据颜色不褪色确定二氧化硫除净,故选①③⑥。