题目内容
A、B、C、D、E为五种元素的单质,其余为化合物.其中只有E为金属 元素,五种元素的原子序数按B、D、C、A、E顺序依次增大,D、C元素在周期表中位置相邻,在一定条件下,B可以分别和A、C、D化合生成甲、乙、丙,C和D化合可得丁.已知乙、丙每个分子中均含有10个电子,图1为相互转化关系:

谘回答下列问题:
(1)图2是周期表的一部分,请将A、C、E用元素符号填在相应的位置上.
(2)写出工业上制取A反应的离子方程式 .
(3)戊的分子式为 .B与D形成的原子个数比为2:1的化合物中,D原子最外层为8电子结构,请写出该化合物的电子式 .
(4)A与丙常温下发生反应生成甲与单质D,该反应的化学方程式 .
(5 )8gE在A中燃烧放出热量QkJ,写出该反应热化学方程式 (热量是常温下测定的).
(6)实验室配制庚溶液的实验方法是 .

谘回答下列问题:
(1)图2是周期表的一部分,请将A、C、E用元素符号填在相应的位置上.
(2)写出工业上制取A反应的离子方程式
(3)戊的分子式为
(4)A与丙常温下发生反应生成甲与单质D,该反应的化学方程式
(5 )8gE在A中燃烧放出热量QkJ,写出该反应热化学方程式
(6)实验室配制庚溶液的实验方法是
分析:B可以分别和C、D化合生成乙、丙,且乙、丙每个分子中均含有10个电子,乙、丙都含有氢元素,由于乙、丙为二元化合物,故B为氢气;D、C元素在周期表中位置相邻,由转化关系中,C与氢化物丙可以反应,则C为氧气,故乙为水;原子序数D<C,则D为氮气、丙为NH3,C和D化合可得丁为NO;B和A化合生成甲为氢化物,由转化关系中A与水反应得到化合物甲、戊,戊在光照分解得到甲与氧气,考虑戊为HClO,则A为Cl2、甲为HCl,E为金属与氯气反应生成己,己与E反应生成庚,E为变价金属,则E为Fe、己为FeCl3,庚为FeCl2,据此解答.
解答:解:B可以分别和C、D化合生成乙、丙,且乙、丙每个分子中均含有10个电子,乙、丙都含有氢元素,由于乙、丙为二元化合物,故B为氢气;D、C元素在周期表中位置相邻,由转化关系中,C与氢化物丙可以反应,则C为氧气,故乙为水;原子序数D<C,则D为氮气、丙为NH3,C和D化合可得丁为NO;B和A化合生成甲为氢化物,由转化关系中A与水反应得到化合物甲、戊,戊在光照分解得到甲与氧气,考虑戊为HClO,则A为Cl2、甲为HCl,E为金属与氯气反应生成己,己与E反应生成庚,E为变价金属,则E为Fe、己为FeCl3,庚为FeCl2,
(1)A、C、E对应的元素分别为Cl、O、Fe,在周期表中的位置为: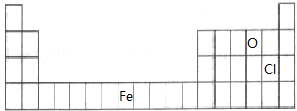 ,
,
故答案为: ;
;
(2)工业上电解饱和食盐水制取氯气,反应的离子方程式为2Cl-+2H2O
Cl2↑+H2↑+2OH-,
故答案为:2Cl-+2H2O
Cl2↑+H2↑+2OH-;
(3)由上述分析可知,戊的分子式为HClO.H与N形成的原子个数比为2:1的化合物为N2H4,N原子最外层为8电子结构,其电子式为 ,
,
故答案为:HClO; ;
;
(4)Cl2与NH3常温下发生反应生成HCl甲与N2,该反应的化学方程式为3Cl2+2NH3=6HCl+N2,故答案为:3Cl2+2NH3=6HCl+N2;
(5 )8gFe在氯气中燃烧放出热量QkJ,2molFe反应放出热量为QkJ×
=14QkJ,故该反应热化学方程式为:2Fe(s)+3Cl2(g)=FeCl3(s)△H=-14QkJ?mol-1,
故答案为:2Fe(s)+3Cl2(g)=FeCl3(s)△H=-14QkJ?mol-1;
(6)实验室配制氯化亚铁溶液,要加入盐酸防止水解,加入铁粉防止氧化,具体实验方法是:向盐酸中加入适量的FeCl2晶体,搅拌溶解,然后加水稀释,并加入少许铁粉,故答案为:向盐酸中加入适量的FeCl2晶体,搅拌溶解,然后加水稀释,并加入少许铁粉.
(1)A、C、E对应的元素分别为Cl、O、Fe,在周期表中的位置为:
 ,
,故答案为:
 ;
;(2)工业上电解饱和食盐水制取氯气,反应的离子方程式为2Cl-+2H2O
| ||
故答案为:2Cl-+2H2O
| ||
(3)由上述分析可知,戊的分子式为HClO.H与N形成的原子个数比为2:1的化合物为N2H4,N原子最外层为8电子结构,其电子式为
 ,
,故答案为:HClO;
 ;
;(4)Cl2与NH3常温下发生反应生成HCl甲与N2,该反应的化学方程式为3Cl2+2NH3=6HCl+N2,故答案为:3Cl2+2NH3=6HCl+N2;
(5 )8gFe在氯气中燃烧放出热量QkJ,2molFe反应放出热量为QkJ×
| 2mol×56g/mol |
| 8g |
故答案为:2Fe(s)+3Cl2(g)=FeCl3(s)△H=-14QkJ?mol-1;
(6)实验室配制氯化亚铁溶液,要加入盐酸防止水解,加入铁粉防止氧化,具体实验方法是:向盐酸中加入适量的FeCl2晶体,搅拌溶解,然后加水稀释,并加入少许铁粉,故答案为:向盐酸中加入适量的FeCl2晶体,搅拌溶解,然后加水稀释,并加入少许铁粉.
点评:本题考查无机物推断、电子式及热化学方程式等常用化学用语、化学实验等知识,乙、丙为10电子物质是推断突破口,对学生的逻辑推理有一定的要求,需要学生熟练掌握元素化合物知识,难度较大,(6)中注意铁盐、亚铁盐溶液的配制.

练习册系列答案
相关题目
【化学--选修3:物质结构与性质】
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)G位于 族 区,价电子排布式为 .
(2)B基态原子中能量最高的电子,其电子云在空间有 个方向,原子轨道呈
形.
(3)画出C原子的电子排布图 .
(4)已知BA5为离子化合物,写出其电子式 .
(5)DE3中心原子的杂化方式为 ,用价层电子对互斥理论推测其空间构型为 .
(6)用电子式表示F元素与E元素形成化合物的形成过程 .
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
形.
(3)画出C原子的电子排布图
(4)已知BA5为离子化合物,写出其电子式
(5)DE3中心原子的杂化方式为
(6)用电子式表示F元素与E元素形成化合物的形成过程
 A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答:
A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答:

