��Ŀ����
����Ŀ��һ���¶�ѹǿ�£����ݻ��ɱ���ܱ������з�����ӦCO(g)+H2O(g)![]() CO2(g)+H2(g) ��H��0��������˵������ȷ����
CO2(g)+H2(g) ��H��0��������˵������ȷ����
A.�����������䣬�Ӵ����벻�Ӵ�������H ��ͬ
B.���ﵽƽ�⣬����ϵ�г���CO2��ƽ�������ƶ�
C.�����ϸ÷�Ӧ����Ƴ�ȼ�ϵ�أ�H2O(g)�������Ϸ�����ԭ��Ӧ
D.ƽ��������ͨ��NaOH��Һǡ�÷�Ӧ�������¶���Һ������ǿ����pHһ������
���𰸡�D
��������
A.����ֻ�ı䷴Ӧ�Ŀ��������ܸı䷴Ӧ����ЧӦ��A�ԣ���ѡ��
B.���ﵽƽ��ʱ������ϵ�г���CO2���������Ũ������ƽ�������ƶ���B�ԣ���ѡ��
C.�÷�Ӧ��������ԭ��Ӧ��������Ƴ�ԭ��أ�H2O(g)��H�Ļ��ϼ۽��ͣ���H2O(g)�������Ϸ�����ԭ��Ӧ��C�ԣ���ѡ��
D.ƽ��������ͨ��NaOH��Һǡ�÷�Ӧ����Na2CO3��Na2CO3ˮ����Һ�Լ��ԣ������¶ȷ����˸ı䣬��Һ������ǿ����pH��һ������D����ѡD��
�ʴ�ѡD��

 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�����Ŀ������β���к���CO��NO���к����塣
��1������β����NO���ɹ��̵������仯��ͼʾ��1molN2��1molO2��ȫ��Ӧ����NO��____�����������������ų�����____kJ������

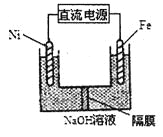
��2��ͨ��NO�������ɼ������β����NO�ĺ������乤��ԭ����ͼ��ʾ������ʾ��O2-���ڴ˹��������������ƶ���

��NiO�缫�Ϸ�������___________��Ӧ������������������ԭ������
�����·�У������Ǵ�_________�缫����������NiO������Pt������
��Pt�缫�ϵĵ缫��ӦʽΪ________________________��
��3��һ�����ʹ�������NO��CO�ķ�Ӧ��2NO+2CO![]() 2CO2+N2����֪��������ıȱ��������߸÷�Ӧ���ʣ�Ϊ����֤�¶ȡ������ıȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ���������ʵ�飬���������Ѿ������±��С�
2CO2+N2����֪��������ıȱ��������߸÷�Ӧ���ʣ�Ϊ����֤�¶ȡ������ıȱ�����Ի�ѧ��Ӧ���ʵ�Ӱ����ɣ�ijͬѧ���������ʵ�飬���������Ѿ������±��С�
ʵ���� | t���棩 | NO��ʼŨ�� ��mol/L�� | CO��ʼŨ�ȣ�mol/L�� | �����ıȱ������m2/g�� |
�� | 280 | 1.2��10��3 | 5.80��10��3 | 82 |
�� | 280 | 1.2��10��3 | b | 124 |
�� | 350 | a | 5.80��10��3 | 82 |
���뽫�������ݲ���������a ___________��
������֤�¶ȶԻ�ѧ��Ӧ���ʹ��ɵ���ʵ��____________����ʵ����ţ���
��ʵ����ʵ����У�NO�����ʵ���Ũ��c��NO����ʱ��t�ı仯������ͼ��ʾ�����б�ʾʵ����������_______����������������������

��4�����ݻ��̶��ľ��������з�����Ӧ2NO+2CO2CO2+N2������˵���Ѵﵽƽ��״̬����________��������ѡ��
A�������ڻ�������¶Ȳ��ٱ仯 B�������ڵ�����ѹǿ���ֲ���
C��2����(NO)=����(N2) D�������ڻ�������ܶȱ��ֲ���