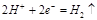题目内容
下列叙述中正确的是
- A.H2SO4的摩尔质量是98
- B.等质量的O2和O3中所含的氧原子个数相等
- C.等质量的CO2和CO中所含有的碳原子个数相等
- D.将98g H2SO4溶解于500mL水中,所得溶液中H2SO4的物质的量浓度为2mol/L
B
分析:A、摩尔质量的单位g/mol;
B、利用n= 及分子的构成来分析;
及分子的构成来分析;
C、利用n= 及分子的构成来分析;
及分子的构成来分析;
D、利用n= 及c=
及c= 来计算浓度,并区分水的体积与溶液的体积.
来计算浓度,并区分水的体积与溶液的体积.
解答:A、H2SO4的摩尔质量是98g/mol,故A错误;
B、若质量都是mg,则O2和O3中所含的氧原子物质的量分别为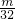 ×2mol、
×2mol、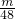 ×3mol,二者相等,则氧原子个数相等,故B正确;
×3mol,二者相等,则氧原子个数相等,故B正确;
C、若质量都是mg,CO2和CO中所含有的碳原子的物质的量分别为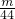 mol×1、
mol×1、 mol×1,二者不相等,则碳原子个数不相等,故C错误;
mol×1,二者不相等,则碳原子个数不相等,故C错误;
D、硫酸的物质的量为 =1mol,H2SO4的物质的量浓度为c=
=1mol,H2SO4的物质的量浓度为c=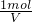 ,水的体积不是溶液的体积,则无法计算,故D错误;
,水的体积不是溶液的体积,则无法计算,故D错误;
故选B.
点评:本题考查有关物质的量的计算,明确以物质的量为中心的计算公式即可解答,本题中的D项是学生的易错点.
分析:A、摩尔质量的单位g/mol;
B、利用n=
 及分子的构成来分析;
及分子的构成来分析;C、利用n=
 及分子的构成来分析;
及分子的构成来分析;D、利用n=
 及c=
及c= 来计算浓度,并区分水的体积与溶液的体积.
来计算浓度,并区分水的体积与溶液的体积.解答:A、H2SO4的摩尔质量是98g/mol,故A错误;
B、若质量都是mg,则O2和O3中所含的氧原子物质的量分别为
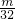 ×2mol、
×2mol、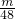 ×3mol,二者相等,则氧原子个数相等,故B正确;
×3mol,二者相等,则氧原子个数相等,故B正确;C、若质量都是mg,CO2和CO中所含有的碳原子的物质的量分别为
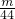 mol×1、
mol×1、 mol×1,二者不相等,则碳原子个数不相等,故C错误;
mol×1,二者不相等,则碳原子个数不相等,故C错误;D、硫酸的物质的量为
 =1mol,H2SO4的物质的量浓度为c=
=1mol,H2SO4的物质的量浓度为c=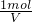 ,水的体积不是溶液的体积,则无法计算,故D错误;
,水的体积不是溶液的体积,则无法计算,故D错误;故选B.
点评:本题考查有关物质的量的计算,明确以物质的量为中心的计算公式即可解答,本题中的D项是学生的易错点.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
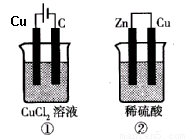
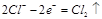 ②中负极
②中负极