题目内容
4.只用一种试剂即可区别苯、甲苯、四氯化碳、氢氧化钠溶液,此试剂是( )| A. | 酸性高锰酸钾溶液 | B. | 溴水 | ||
| C. | 浓硫酸 | D. | 液溴 |
分析 A、苯与高锰酸钾溶液不反应且分层;甲苯能被高锰酸钾溶液氧化;四氯化碳不和高锰酸钾溶液反应且分层;氢氧化钠与高锰酸钾溶液不反应且不分层;
B、苯和甲苯均与溴水不反应,发生萃取;
C、苯、甲苯与浓硫酸均不反应,且分层;
D、液溴均易溶于苯、甲苯和四氯化碳.
解答 解:A、苯与高锰酸钾溶液不反应且分层,由于苯的密度小于水,故苯在上层;甲苯能被高锰酸钾溶液氧化,使高锰酸钾溶液褪色;四氯化碳不和高锰酸钾溶液反应且分层,由于四氯化碳密度比水大,故油状液体在下层;氢氧化钠与高锰酸钾溶液不反应且不分层,故四种物质与高锰酸钾溶液混合后现象均不同,故可以用高锰酸钾溶液鉴别开,故A正确;
B、苯和甲苯均与溴水不反应,均发生萃取,且由于苯和甲苯的密度比水小,故萃取后,溴的苯和溴的甲苯溶液均在上层,区分不开,故B错误;
C、苯、甲苯与浓硫酸均不反应,混合后分层,且由于苯和甲苯的密度均比水小,故苯和甲苯均在浓硫酸的上层,区分不开,故C错误;
D、液溴均易溶于苯、甲苯和四氯化碳,故混合后均得橙红色溴的有机溶液,区分不开,故D错误.
故选A.
点评 本题考查有机物的鉴别,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握物质的性质的异同,为解答该题的关键,难度不大.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
14.氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸;在
空气中迅速被氧化成绿色;见光则分解,变成褐色;下图是工业上以制作印刷电路的废液(含Fe3+、Cu2+、
Fe2+、Cl-)生产CuCl的流程如下:
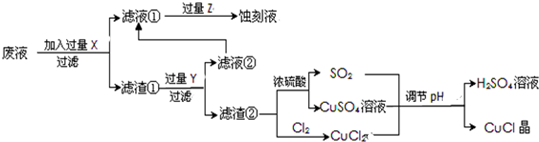
根据以上信息回答下列问题:
(1)该生产过程还可以与氯碱工业、硫酸工业生产相结合,工业生产硫酸的方法名称是接触室,现代氯碱工业的装置名称是离子交换膜电解槽.
(2)写出生产过程中XFeYHCl (填化学式)
(3)写出产生CuCl的化学方程式CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4.
(4)生产中为了提高CuCl产品的质量,采用抽滤或者减压过滤,法快速过滤,析出的CuCl晶体不用水而用无水乙醇洗涤的目的是减少CuCl的损失;生产过程中调节溶液的pH不能过大的原因是防止CuCl水解.
(5)在CuCl的生成过程中理论上不需要补充SO2气体,其理由是Cu+2 H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O反应中生成的CuSO4和 SO2为1:1,CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2 H2SO4反应中消耗CuSO4和SO2也为1﹕1,所以理论上不需要补充SO2气体.
(6)在CuCl的生成过程中除环境问题、安全问题外,还应该注意的关键问题是防止CuCl的氧化和见光分解.
(7)工业氯化亚铜的定量分析:
①称取样品0.25g(称准至0.0002g)置于预先放入玻璃珠50粒和10ml过量的FeCl3溶液250ml锥形瓶中,不断摇动;玻璃珠的作用是加速固体的溶解.
②待样品溶解后,加水50ml,邻菲罗啉指示剂2滴;
③立即用0.10mol•L-1硫酸铈标准溶液滴至绿色出现为终点;同时做空白试验一次.已知:CuCl+FeCl3═CuCl2+FeCl2 Fe2++Ce4+═Fe3++Ce3+如此再重复二次测得:
④数据处理:计算得该工业CuCl的纯度为95%(平行实验结果相差不能超过0.3%)
空气中迅速被氧化成绿色;见光则分解,变成褐色;下图是工业上以制作印刷电路的废液(含Fe3+、Cu2+、
Fe2+、Cl-)生产CuCl的流程如下:

根据以上信息回答下列问题:
(1)该生产过程还可以与氯碱工业、硫酸工业生产相结合,工业生产硫酸的方法名称是接触室,现代氯碱工业的装置名称是离子交换膜电解槽.
(2)写出生产过程中XFeYHCl (填化学式)
(3)写出产生CuCl的化学方程式CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2H2SO4.
(4)生产中为了提高CuCl产品的质量,采用抽滤或者减压过滤,法快速过滤,析出的CuCl晶体不用水而用无水乙醇洗涤的目的是减少CuCl的损失;生产过程中调节溶液的pH不能过大的原因是防止CuCl水解.
(5)在CuCl的生成过程中理论上不需要补充SO2气体,其理由是Cu+2 H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O反应中生成的CuSO4和 SO2为1:1,CuCl2+CuSO4+SO2+2H2O=2CuCl↓+2 H2SO4反应中消耗CuSO4和SO2也为1﹕1,所以理论上不需要补充SO2气体.
(6)在CuCl的生成过程中除环境问题、安全问题外,还应该注意的关键问题是防止CuCl的氧化和见光分解.
(7)工业氯化亚铜的定量分析:
①称取样品0.25g(称准至0.0002g)置于预先放入玻璃珠50粒和10ml过量的FeCl3溶液250ml锥形瓶中,不断摇动;玻璃珠的作用是加速固体的溶解.
②待样品溶解后,加水50ml,邻菲罗啉指示剂2滴;
③立即用0.10mol•L-1硫酸铈标准溶液滴至绿色出现为终点;同时做空白试验一次.已知:CuCl+FeCl3═CuCl2+FeCl2 Fe2++Ce4+═Fe3++Ce3+如此再重复二次测得:
| 1 | 2 | 3 | |
| 空白实验消耗硫酸铈标准溶液的体积(ml) | 0.75 | 0.50 | 0.80 |
| 0.25克样品消耗硫酸铈标准溶液的体积(ml) | 24.65 | 24.75 | 24.70 |
15.下列说法或表示正确的是( )
| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量少 | |
| B. | 由单质A转化为单质B时△H=+119 kJ•mol-1可知单质B比单质A稳定 | |
| C. | 稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ | |
| D. | 在101 kPa时,H2燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1,则H2在101 kPa时的燃烧热为571.6 kJ•mol-1 |
19.下列有关离子方程式书写正确的( )
| A. | 向含1molFeI2溶液中通入标准状况下22.4LCl22Fe2++2I-+2Cl2=2Fe3++I2+2Cl- | |
| B. | 在Na2S溶液中滴加少量FeCl3 2Fe3++S2-═2Fe2++S↓ | |
| C. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O=C6H5OH+HSO${\;}_{3}^{-}$ |
13.下列变化中,必须要加入氧化剂才能实现的是( )
| A. | Na2O2→O2 | B. | FeCl2→FeCl3 | C. | HCl→H2 | D. | SO3→H2SO4 |

 某实验需要100mL、0.1mol/L的Na2CO3溶液,现通过如下操作配制:
某实验需要100mL、0.1mol/L的Na2CO3溶液,现通过如下操作配制: