题目内容
【题目】过二硫酸铵![]() 是一种常用的氧化剂和漂白剂。某小组以辉铜矿(主要成分是
是一种常用的氧化剂和漂白剂。某小组以辉铜矿(主要成分是![]() )为原料用火法炼铜,并利用尾气制备过二硫酸铵。模拟工艺流程如下:
)为原料用火法炼铜,并利用尾气制备过二硫酸铵。模拟工艺流程如下:
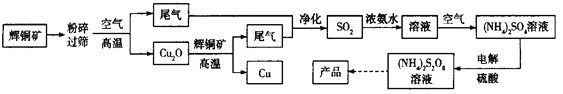
(1)矿石“粉碎过筛”的目的是_________。
(2)已知常温下![]() 的
的![]() ,
,![]() ,
,![]() 的
的![]() 。若浓氨水吸收
。若浓氨水吸收![]() 恰好生成
恰好生成![]() 溶液,则该溶液的pH__________(填“>”“<”或“=”)7。
溶液,则该溶液的pH__________(填“>”“<”或“=”)7。
(3)![]() 和
和![]() 按一定比例混合,在高温下反应的化学方程式为_______该反应中的氧化剂是_______(填化学式)。
按一定比例混合,在高温下反应的化学方程式为_______该反应中的氧化剂是_______(填化学式)。
(4)过二硫酸铵常用于检验废水中![]() 是否超标,若超标则溶液变为橙色(还原产物为
是否超标,若超标则溶液变为橙色(还原产物为![]() ),写出该反应的离子方程式:__________________。
),写出该反应的离子方程式:__________________。
(5)工业上,常采用钛基镀铂电极为阳极,铅锑合金为阴极,用质子交换膜将电解池分成两个室,将硫酸铵和硫酸分别加入到两个电极室进行电解制备过二硫酸铵,硫酸放入阴极室。写出阳极的电极反应式:___。
【答案】增大固体与气体的接触面积,加快反应速率 < ![]()
![]() 、
、![]()
![]()
![]()
【解析】
流程将粉碎的辉铜矿在空气中高温煅烧得氧化亚铜和二氧化硫,氧化亚铜和辉铜矿反应生成铜和二氧化硫,方程式为2Cu2O+Cu2S![]() 6Cu+SO2↑,将二氧化硫净化后用浓氨水吸收得到NH4HSO3,NH4HSO3在空气中被氧化为硫酸铵,将硫酸铵和硫酸分别加入到两个电极室进行电解制备过二硫酸铵,据此分析。
6Cu+SO2↑,将二氧化硫净化后用浓氨水吸收得到NH4HSO3,NH4HSO3在空气中被氧化为硫酸铵,将硫酸铵和硫酸分别加入到两个电极室进行电解制备过二硫酸铵,据此分析。
(1)粉碎矿石过筛,可以增大固体与气体的接触面积,加快固体与气体的反应速率;
答案:增大固体与气体的接触面积,加快反应速率
(2)![]() 的pKh=14-pKa1=12.19>pK a2,故其电离程度大于水解程度,又由于NH4+水解呈酸性,所以NH4HSO3溶液呈酸性;
的pKh=14-pKa1=12.19>pK a2,故其电离程度大于水解程度,又由于NH4+水解呈酸性,所以NH4HSO3溶液呈酸性;
答案:<
(3)氧化亚铜和辉铜矿反应生成铜和二氧化硫,方程式为2Cu2O+Cu2S![]() 6Cu+SO2↑,Cu2O、Cu2S中铜的化合价都降低,它们都是氧化剂;
6Cu+SO2↑,Cu2O、Cu2S中铜的化合价都降低,它们都是氧化剂;
答案:Cu2O、Cu2S
(4)由题意,反应物为Cr3+、S2O82-和H2O,生成物为Cr2O72-、SO42-和![]() 。根据得失电子守恒,电荷守恒和元素守恒书写离子方程式2Cr3++3 S2O82-+7H2O= Cr2O72-+6 SO42-+14H+;
。根据得失电子守恒,电荷守恒和元素守恒书写离子方程式2Cr3++3 S2O82-+7H2O= Cr2O72-+6 SO42-+14H+;
答案: 2Cr3++3 S2O82-+7H2O= Cr2O72-+6 SO42-+14H+
(5)阳极上硫酸根离子被氧化为S2O82-,电极反应式为2SO42—2e-= S2O82-;
答案:2SO42—2e-= S2O82-

 金钥匙试卷系列答案
金钥匙试卷系列答案【题目】对甲烷和CO2的高效利用不仅能缓解大气变暖,而且对日益枯竭的石油资源也有一定的补充作用,甲烷临氧耦合CO2重整反应有:
反应(i):2CH4(g)+O2(g)![]() 2CO(g)+4H2(g) △H=-71.4kJmol-1
2CO(g)+4H2(g) △H=-71.4kJmol-1
反应(ii):CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) △H=+247.0 kJmol-1
2CO(g)+2H2(g) △H=+247.0 kJmol-1
(1)写出表示CO燃烧热的热化学方程式:_______________________________。
(2)在两个体积均为2L的恒容密闭容器中,起始时按表中相应的量加入物质,在相同温度下进行反应(ii):CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) (不发生其它反应),CO2的平衡转化率如下表所示:
2CO(g)+2H2(g) (不发生其它反应),CO2的平衡转化率如下表所示:
容器 | 起始物质的量(n) / mol | CO2的 平衡转化率 | |||
CH4 | CO2 | CO | H2 | ||
Ⅰ | 0.1 | 0.1 | 0 | 0 | 50% |
Ⅱ | 0.1 | 0.1 | 0.2 | 0.2 | / |
①下列能说明反应达到平衡状态是_________。
A.v正(CH4) =2v逆(CO)
B.容器内各物质的浓度满足c(CH4)·c(CO2)=c2(CO)·c2(H2)
C.容器内混合气体的总压强不再变化
D.容器内混合气体密度保持不变
②若容器Ⅰ内反应从开始到平衡所用的时间为t min,则t min内该反应的平均反应速率为:v(H2) = ________(用含t的表达式表示)。
③达到平衡时,容器Ⅰ、Ⅱ内CO的物质的量的关系满足:2n(CO)Ⅰ_______n(CO)Ⅱ(填“>”、“=”或“<”)
(3)将CH4(g)和O2(g)以物质的量比为4:3充入盛有催化剂的恒容密闭容器内,发生上述反应(i):2CH4(g)+O2(g)![]() 2CO(g)+4H2(g),相同时间段内测得CO的体积分数[ψ(CO)]与温度(T)的关系如图如示。
2CO(g)+4H2(g),相同时间段内测得CO的体积分数[ψ(CO)]与温度(T)的关系如图如示。
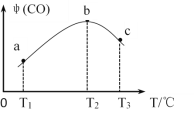
① T2℃时,CO体积分数最大的原因是_____________。
②若T2℃时,容器内起始压强为P0,平衡时CO的体积分数为20%,则反应的平衡常数KP =_______(用平衡分压强代替平衡浓度计算,分压=总压×物质的量分数)。
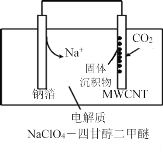
(4)2016年我国科研人员根据反应Na+CO2→ Na2CO3+C(未配平) 研制出一种室温“可呼吸”Na-CO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。其放电时的工作原理如图所示,已知吸收的全部CO2中,有![]() 转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面,写出放电时正极的电极反应式:_________________。
转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面,写出放电时正极的电极反应式:_________________。
【题目】下列实验操作、解释或结论均正确的是
选项 | 实验目的 | 操作 | 结论或解释 |
A | 检验 | 取待测液少许,加入过量的 | 液体分层,加入硝酸酸化的 |
B | 检验某溶液中有无 | 取待测液少许,加入盐酸,有气体放出,将气体通入澄清石灰水中 | 澄清石灰水变浑浊,则含 |
C | 检验溶液中的 | 取待测液少许,先通入氯气,再加KSCN溶液 | 溶液变红色,则含 |
D | 检验食盐中是否含 | 取少量食盐溶于水,加少量淀粉 | 溶液变蓝色,则含 |
A.AB.BC.CD.D
【题目】燃煤的烟气中含有 SO2,为了治理雾霾天气,工厂采用多种方法实现烟气脱硫。
Ⅰ.(1)“湿式吸收法”利用吸收剂与 SO2 发生反应从而脱硫。下列试剂中适合用作该法吸收剂的是_____(填字母序号)。
a. 石灰乳 b.CaCl2溶液
(2)某工厂利用含 SO2 的烟气处理含Cr2O72-的酸性废水,吸收塔中反应后的铬元素以Cr3+形式存在,具体流程如下:

①用 SO2 处理含铬废水时,利用了 SO2 的_____性。
②吸收塔中发生反应的离子方程式为_____。
Ⅱ.石灰-石膏法和烧碱法是常用的烟气脱硫法。石灰-石膏法的吸收反应为Ca(OH)2+SO2= CaSO3↓+H2O。吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O =2CaSO4·2H2O。其流程如图:

烧碱法的吸收反应为2NaOH+SO2=Na2SO3+H2O。该法的特点是氢氧化钠碱性强、吸收快、效率高。其流程如图:

已知:
试剂 | Ca(OH)2 | NaOH |
价格(元/kg) | 0.36 | 2.9 |
吸收 SO2 的成本(元/mol) | 0.027 | 0.232 |
(3)石灰-石膏法和烧碱法相比,石灰-石膏法的优点是_______,缺点是_______。
(4)某学习小组在石灰-石膏法和烧碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案,流程图中的甲、乙、丙各是_____、_____、_____(填化学式)