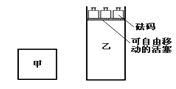
题目内容
【题目】请回答下列问题:
(1)有以下几种物质① NaCl晶体 ②液态氯化氢 ③铜丝 ④SiO2 ⑤NH3 ⑥KNO3溶液 填空回答(填序号):以上物质中能导电的是 ;属于电解质的是 ;属于非电解质的是 ;上述纯净物中含有共价键的是 ;既不是电解质也不是非电解质的是 。
(2)A、B、C、D、E、F六种物质含有同一种元素,六种物质的相互转化关系如下,E是淡黄色粉末,判断:
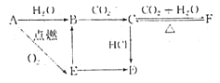
写出有关反应的化学方程式(是离子反应的直接写出离子方程式)
B→C:_________________________;E→B:________________________;
C→F:_________________________;F→C:_________________________。
【答案】
(1)③⑥ ①② ④⑤ ②④⑤ ③⑥
(2)B→C:2OH-+CO2=CO32-+H2O
E→B:2Na2O2+2H2O=4Na++4OH-+O2↑
C→F:CO32-+CO2+H2O=2HCO3-
F→C:2NaHCO3=Na2CO3+H2O+CO2↑
【解析】
试题分析:(1)能导电的物质必须有能够自由移动的带电的微粒,金属铜中存在能自由移动的带负电的电子能导电,KNO3溶液中有能自由移动的阴阳离子,也能导电,所以以上物质中能导电的是③⑥;电解质是在水溶液中或熔融状态下能够导电的化合物,则属于电解质的是①②;非电解质是在水溶液中和熔融状态下都不能能够导电的化合物,则属于非电解质的是④⑤;共价键是由非金属元素通过共用电子对形成的物质,则上述纯净物中含有共价键的是②④⑤;混合物和单质既不是电解质,也不是非电解质,则既不是电解质也不是非电解质的是③⑥。
(2)E是淡黄色粉末,A与氧气反应生成淡黄色粉末,则A为Na,E为Na2O2,Na与水反应生成NaOH和氢气,则B为NaOH,NaOH与CO2反应生成碳酸钠,碳酸钠与CO2反应生成碳酸氢钠,则C为Na2CO3,F为NaHCO3 ,碳酸氢钠受热分解生成碳酸钠、CO2和水,碳酸钠与HCl反应生成氯化钠,则D为NaCl。根据离子方程式的书写规则书写,则B→C:2OH-+CO2=CO32-+H2O;E→B: 2Na2O2+2H2O =4Na++4OH-+O2↑;C→F:CO32-+CO2+H2O=2HCO3- ;F→C: 2NaHCO3 =Na2CO3+H2O+CO2↑。

【题目】
成分 | 质量(g) | 摩尔质量(g ·mol-1) |
蔗糖 | 50.00 | 342 |
硫酸钾 | 0.50 | 174 |
阿司匹林 | 0.35 | 180 |
高锰酸钾 | 0.50 | 158 |
硝酸银 | 0.04 | 170 |
⑴下列“鲜花保鲜剂”的成分中,属于非电解质的是 。
A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银
⑵“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为 mol.L-1。(只要求写表达式,不需要计算)
⑶配制上述1 L“鲜花保鲜剂”所需的仪器有:烧杯、玻璃棒、药匙、 、 、 。(在横线上填写所缺仪器的名称)
⑷在溶液配制过程中,下列操作正确且对配制结果没有影响的是 。
A.将药品放入容量瓶中加蒸馏水溶解
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理