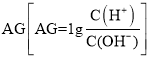题目内容
【题目】甲醇是重要的化工原料,又可作为燃料,工业上可利用CO或CO2来生产燃料甲醇。已知制备甲醇的有关反应的化学方程式及其在不同温度下的化学平衡常数如表所示。
化学反应 | 化学平衡常数 | 温度(℃) | ||
500 | 700 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.34 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 1.70 | 2.52 |
③3H2(g)+CO2(g) | K3 | |||
(1)下列措施能使反应③的平衡体系中![]() 增大的是__
增大的是__
A.将H2O(g)从体系中分离出去 B.恒容时充入He(g),使体系压强增大
C.升高温度 D.恒容时再充入1molH2(g)
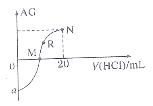
(2)T℃时,反应③在恒容密闭容器中充入1molCO2和nmolH2,混合气体中CH3OH的体积分数与氢气的物质的量的关系如图1所示。图1中A、B、C三点对应的体系,CO2的转化率最大的是___(填字母)。
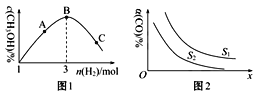
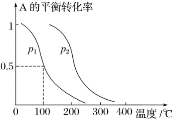
(3)工业上也用合成气(H2和CO)合成甲醇,反应为2H2(g)+CO(g)![]() CH3OH(g) ΔH<0,在10L的恒容密闭容器中充入H2和C物质的量比为2:1,测得CO的平衡转化率与温度、压强的关系如图2所示。
CH3OH(g) ΔH<0,在10L的恒容密闭容器中充入H2和C物质的量比为2:1,测得CO的平衡转化率与温度、压强的关系如图2所示。
①图2中S代表的物理量是___。
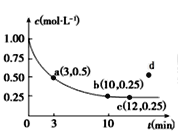
②300℃时,氢气的物质的量随时间变化如表所示
反应时间/min | 0 | 1 | 4 | 5 |
H2/mol | 8 | 5.4 | 4 | 4 |
在该温度下,上述反应的平衡常数为___。若再向该平衡体系中再加入2molCO、2molH2、2molCH3OH,保持温度和容器体积不变,则平衡会___(填“正向移动”“逆向移动”或“不移动”)。
【答案】AD C 压强 6.25L2/mol2 正向移动
【解析】
(1).A.将H2O(g)从体系中分离出去,减小H2O(g)的浓度,平衡正向移动,n(CH3OH)增大、n(CO2)减小,所以![]() 增大,故A正确;
增大,故A正确;
B.充入He(g),使体系压强增大,因不能改变平衡体系中各物质的浓度,所以平衡不移动,则![]() 不变,故B错误;
不变,故B错误;
C.根据上述分析可知,K3=K1×K2,则K3在500℃、700℃、800℃时的数值分别为:2.5、0.58、0.38,说明随温度的升高,平衡常数减小,则反应③是放热反应,则升高温度平衡逆向移动,n(CH3OH)减小、n(CO2)增大,所以![]() 减小,故C错误;
减小,故C错误;
D. 再充入1mol H2,平衡正向移动,n(CH3OH)增大、n(CO2)减小,所以![]() 增大,故D正确;
增大,故D正确;
答案选AD;
(2)增大氢气的量,CO2的转化率增大,C点时氢气的量最大,故CO2的转化率最大;答案选C;
(2)①反应2H2(g)+CO(g)![]() CH3OH(g) ΔH<0的正反应是气体体积减小的放热反应,升高温度,平衡逆向移动,CO的平衡转化率减小。增大压强,平衡正向移动,CO的平衡转化率增大,故S代表的物理量是压强;
CH3OH(g) ΔH<0的正反应是气体体积减小的放热反应,升高温度,平衡逆向移动,CO的平衡转化率减小。增大压强,平衡正向移动,CO的平衡转化率增大,故S代表的物理量是压强;
②300℃时,根据表中数据及三段式可知,
2H2(g)+CO(g)![]() CH3OH(g)
CH3OH(g)
起始量(mol/L) 0.8 0.4 0
变化量(mol/L) 0.4 0.2 0.2
平衡量(mol/L) 0.4 0.2 0.2
平衡常数K=![]() =6.25L2/mol2
=6.25L2/mol2
达到平衡后,再向该平衡体系中再加入2molCO、2molH2、 2molCH3OH 若保持温度和容器休积不变,相当于增大压强,平衡将向正反应方向移动。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】硫代硫酸钠(Na2S2O3)是一种解毒药,用于氟化物、砷、汞、铅、锡、碘等中毒,临床常用于治疗荨麻疹,皮肤瘙痒等病症.硫代硫酸钠在中性或碱性环境中稳定,在酸性溶液中分解产生S和SO2
实验I:Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示:

(1)仪器a的名称是_______,仪器b的名称是_______。b中利用质量分数为70%80%的H2SO4溶液与Na2SO3固体反应制备SO2反应的化学方程式为_______。c中试剂为_______
(2)实验中要控制SO2的生成速率,可以采取的措施有_______ (写出一条)
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2不能过量,原因是_______
实验Ⅱ:探究Na2S2O3与金属阳离子的氧化还原反应。
资料:Fe3++3S2O32-Fe(S2O3)33-(紫黑色)
装置 | 试剂X | 实验现象 |
| Fe2(SO4)3溶液 | 混合后溶液先变成紫黑色,30s后几乎变为无色 |
(4)根据上述实验现象,初步判断最终Fe3+被S2O32-还原为Fe2+,通过_______(填操作、试剂和现象),进一步证实生成了Fe2+。从化学反应速率和平衡的角度解释实验Ⅱ的现象:_______
实验Ⅲ:标定Na2S2O3溶液的浓度
(5)称取一定质量的产品配制成硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:用分析天平准确称取基准物质K2Cr2O7(摩尔质量为294gmol-1)0.5880g。平均分成3份,分别放入3个锥形瓶中,加水配成溶液,并加入过量的KI并酸化,发生下列反应:6I-+Cr2O72-+14H+ = 3I2+2Cr3++7H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应I2+2S2O32- = 2I- + S4O62-,三次消耗 Na2S2O3溶液的平均体积为25.00 mL,则所标定的硫代硫酸钠溶液的浓度为_______molL-1