题目内容
2. 在工业中利用镁制取硅:2Mg+SiO22MgO+Si,同时有副反应发生:2Mg+SiMg2Si,Mg2Si遇盐酸迅速反应生成SiH4(硅烷),SiH4在常温下是一种不稳定、易分解的气体.如图是进行Mg与SiO2反应的实验装置:
在工业中利用镁制取硅:2Mg+SiO22MgO+Si,同时有副反应发生:2Mg+SiMg2Si,Mg2Si遇盐酸迅速反应生成SiH4(硅烷),SiH4在常温下是一种不稳定、易分解的气体.如图是进行Mg与SiO2反应的实验装置:(1)由于氧气的存在对该实验有较大影响,实验中应通入气体X作为保护气,试管中的固体药品可选用b(填序号).
a.石灰石 b.锌粒 c.纯碱
(2)实验开始时,必须先通入X气体,再加热反应物,其理由是让氢气排尽装置内的空气,避免空气中的成分对实验的影响,
当反应开始后,移走酒精灯反应能继续进行,其原因是该反应为放热反应,可利用自身放出的热量维持反应进行.
(3)反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸.可观察到闪亮的火星,产生此现象的原因用化学方程式表示为
①Mg2Si+4HCl═2MgCl2+SiH4↑;
②SiH4+2O2═SiO2+2H2O.
分析 Mg为活泼金属,在空气中点燃可以和O2、CO2、H2O反应,在工业中利用镁制取硅:需排尽装置中的空气,实验中应通入气体X作为保护气,X由稀硫酸制得,根据题干(1)信息可知,用锌和稀硫酸制得的氢气排空装置中的空气,氢气和空气的混合气体燃烧会发生爆炸,所以反应开始前应该先通氢气排尽装置中的空气,X为氢气,通过浓硫酸进行干燥,当反应开始后,移走酒精灯反应能继续进行,Mg与SiO2反应是放热反应,反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸发生Mg2Si+4HCl═2MgCl2+SiH4↑,
SiH4+2O2═SiO2+2H2O.
(1)Mg可以与CO2、N2发生化学反应,Mg与氢气不能发生反应,依据X为氢气选择药品;
(2)实验开始时应先通入氢气排出装置内的空气,避免空气中的成分对实验的影响,然后才能点燃酒精灯,因反应放热,反应开始后移走酒精灯,可利用自身放出的热量维持反应继续进行;
(3)Mg2Si遇盐酸迅速反应生成SiH4(硅烷),SiH4在常温下是一种不稳定、易自燃的气体,反应结束后,向反应后的混合物中加入稀盐酸会发生反应,Mg2Si与HCl反应生成的SiH4可自燃,所以会观察到闪亮的火星.
解答 解:Mg为活泼金属,在空气中点燃可以和O2、CO2、H2O反应,在工业中利用镁制取硅:需排尽装置中的空气,实验中应通入气体X作为保护气,X由稀硫酸制得,根据题干(1)信息可知,用锌和稀硫酸制得的氢气排空装置中的空气,氢气和空气的混合气体燃烧会发生爆炸,所以反应开始前应该先通氢气排尽装置中的空气,X为氢气,通过浓硫酸进行干燥,当反应开始后,移走酒精灯反应能继续进行,Mg与SiO2反应是放热反应,反应结束后,待冷却至常温时,往反应后的混合物中加入稀盐酸发生Mg2Si+4HCl═2MgCl2+SiH4↑,SiH4+2O2═SiO2+2H2O.
(1)Mg可以与CO2发生化学反应生成氧化镁和碳,Mg与氢气不能发生反应,因此可用氢气作为保护气,选用的药品为稀硫酸和锌粒,再用浓硫酸干燥,所以试管中的固体药品可选用锌粒,
故答案为:b;
(2)装置中有空气,若不用氢气排空装置中的空气,氢气和空气的混合气体燃烧会发生爆炸,所以反应开始前应该先通氢气排尽装置中的空气;Mg与SiO2反应的条件是加热,停止加热后,反应的条件由反应放出的热量维持,
故答案为:让氢气排尽装置内的空气,避免空气中的成分对实验的影响;该反应为放热反应,可利用自身放出的热量维持反应进行;
(3)Mg2Si遇盐酸迅速反应生成SiH4(硅烷),其反应的方程式为:Mg2Si+4HCl═2MgCl2+SiH4↑,SiH4常温下是一种不稳定、易自燃的气体,反应的方程式为SiH4+2O2═SiO2+2H2O,所以往反应后的混合物中加入稀盐酸,可观察到闪亮的火星,
故答案为:Mg2Si+4HCl═2MgCl2+SiH4↑;SiH4+2O2═SiO2+2H2O.
点评 本题考查了物质实验室制备原理和装置选择,实验步骤的设计分析判断,把握物质性质的应用是解题关键,题目难度中等,侧重于考查学生的实验探究能力.

| A. | “另一种反应物”一定只具有氧化性 | B. | “另一种反应物”一定具有还原性 | ||
| C. | 点燃时:2CuH+3Cl2═2CuCl2+2HCl | D. | CuH 既可做氧化剂也可做还原剂 |
| 温度 溶解度 化学式 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| KC104 | 0.76 | 1.06 | 1.68 | 2.56 | 3.73 |
| KC1 | 28 | 31.2 | 34.2 | 37.2 | 40.1 |
| NaClO4 | 167 | 183 | 201 | 222 | 245 |
(2)热电池是以熔盐作电解质,利用热源使其熔化而激活得一次储备电池.Li/FeS2热电池工作时,Li转变为硫化锂,FeS2转变为铁,该电池工作时,电池总反应为FeS2+4Li═Fe+2Li2S.
(3)Fe和KC104反应放出的热量能为熔盐电池提供550-660℃的温度,使低熔点盐熔化导电,从而激活电池,其供热原理为:KClO4(s)+4Fe(s)═KC1(s)+4FeO(s),△H<0.
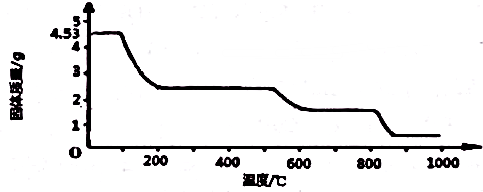
①600℃时FeO可部分分解生成Fe304,写出有关的化学方程式4FeO=Fe3O4+Fe.
②称取一定质量上述加热材料反应后的混合物(假定只含氯化钾一种钾盐)于烧杯中,用蒸馏水充分洗涤、过滤、干燥,固体质量减少了0.43g,在固体中继续加入过量的稀硫酸,微热让其充分反应,固体完全溶解得到的溶液中加入过量的NaOH溶液,经过滤、洗净、干燥,再在空气中充分灼烧得6.0g棕色固体.求该加热材料反应前,铁和高氯酸钾的质量.(写出计算过程,结果保留2位有效数字)铁的质量为4.2g、高氯酸钾的质量为0.80g.
| A. | 电解后,c(Na2SO4)不变,且溶液中有晶体析出 | |
| B. | 电解池的阳极反应式为:4OH--4e-═2H2O+O2↑ | |
| C. | 蓄电池放电时,每消耗0.1molPb,共生成0.1molPbSO4 | |
| D. | 蓄电池中每生成2molH2O,电解池中就消耗1molH2O |