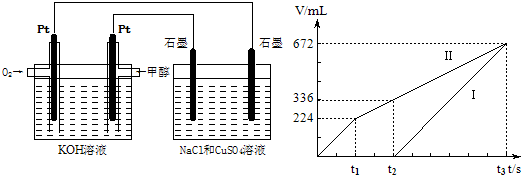
��Ŀ����
��13�֣���Դ��ȱ������������ٵ��ش����⡣�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��1����ҵ��һ������������ַ�Ӧ�ϳɼ״���
��ӦI�� CO(g) �� 2H2(g)  CH3OH(g) ��H1
CH3OH(g) ��H1
��ӦII�� CO2(g) �� 3H2(g)  CH3OH(g) + H2O(g) ��H2
CH3OH(g) + H2O(g) ��H2
��������Ӧ���ϡ�ԭ�Ӿ��á�ԭ����� ���I������
���±����������Ƿ�ӦI�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�ɱ��������жϦ�H1 0 �����������������������
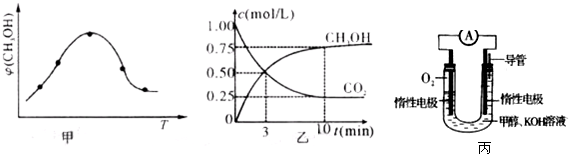
��ij�¶��£���2 mol CO��6 mol H2����2L���ܱ������У���ַ�Ӧ���ﵽƽ����c(CH3OH)�� 0.8 mol��L����CO��ת����Ϊ ����ʱ���¶�Ϊ �����ϱ���ѡ��
�ܺ��¡�����ʱ�������������˵����ӦI�Ѿ��ﵽ��ѧƽ��״̬����________________��
 a�����������ʵ�Ũ�ȱ��ֲ��䣻 b��������ѹǿ���ֲ��䣻
a�����������ʵ�Ũ�ȱ��ֲ��䣻 b��������ѹǿ���ֲ��䣻 c����(CO)����==1/2��(H2)���ɡ� d �������ڵ��ܶȱ��ֲ���
c����(CO)����==1/2��(H2)���ɡ� d �������ڵ��ܶȱ��ֲ�����2��25�桢101kPaʱ��ȼ��16gҺ��״�����CO2��H2O(l)���ų�������Ϊ363.26kJ��д���״�ȼ�յ��Ȼ�ѧ����ʽ�� ��
��3��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ�������һ��ȼ�ϵ�ص��Na2SO4��Һ(ͼ����)�������ͼʾ�ش��������⣺
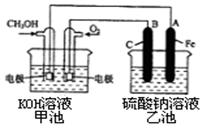
��ͨ��״������ĵ缫ӦΪ ������д�������������� �õ缫�Ϸ����ĵ缫��Ӧ�� ������ĸ���ţ���
a.2CH3OH ��12 e- +3O2 === 2CO2 + 4 H2O
b.CH3OH��6 e- + 8 OH- ="==" CO32- + 6H2O
c.O2 + 2H2O + 4 e- ="==" 4OH- ����������
d.O2�� 4 e- + 4H+ ="==" 2H2O
��д���缫A������ ��д��B�缫�ĵ缫��Ӧʽ ��
�۵����Լ״�ȼ�ϵ������3.36 L ����ʱ���ۺ�Ϊ��״�����������ϵ��Na2SO4��Һ��������������ʵ����� ��
��1���٢� �ڣ� ��80%��250�� ��d
��2��CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ��H=-726.52kJ/mol
��3���ٸ� b ��������4OH-+4e=O2��+2H2O ��0.45mol
����

��ϰ��ϵ�д�
 �����Ļ�������ҵϵ�д�
�����Ļ�������ҵϵ�д� ����������������ϵ�д�
����������������ϵ�д�
�����Ŀ
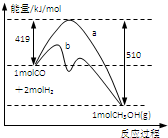 ��Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����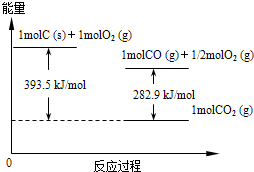 ��2012?������һģ����Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��2012?������һģ����Դ��ȱ������������ٵ��ش����⣮�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����