题目内容
 能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.(1)工业上一般采用下列两种反应合成甲醇:
反应Ⅰ:CO(g)+2H2(g)?CH3OH(g)△H1
反应Ⅱ:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H2
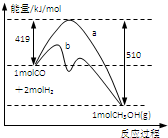
如图所示是反应I反应过程中的能量变化曲线.
(1)由图可知反应I为
放热
放热
反应(选填”吸热、放热”),反应热△H1=-91kJ/mol
-91kJ/mol
.(2)反应I在一定体积的密闭容器中进行,能判断其是否达到化学平衡状态的依据是
AB
AB
.A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(CH3OH)
D.c(CO)=c(CH3OH)
(3)图中曲线
b
b
表示使用催化剂时反应的能量变化.(4)一定条件下,向体积为2L的密闭容器中充入2mol CO2和6mol H2,一段时间后达到平衡状态,测得CH3OH(g)的物质的量为1mol,则此条件下该反应的化学平衡常数数K值=
| 4 |
| 27 |
| 4 |
| 27 |
50%
50%
,若平衡后在充入4mol的N2,则c(CO2)是0.5mol/L
0.5mol/L
.(5)从绿色化学的角度比较上述两种方法,符合原子经济的是
Ⅰ
Ⅰ
.(填“Ⅰ”或“Ⅱ”)分析:(1)根据反应物总能量和生成物总能量的关系判断反应热;根据反应热等于正反应的活化能减去逆反应的活化能;
(2)当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,据此解答,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(3)根据催化剂能降低反应的活化能;
(4)先根据三段式计算出平衡时各物质的浓度,利用各物质平衡的浓度来计算化学平衡常数,利用转化率定义计算CH3OH的转化率;根据等效平衡的从正向建立和逆向建立,转化率之和100%;根据恒容条件下,充入与反应无关的气体,压强增大,平衡不移动,各物质的浓度不变;
(5)原子经济性反应是原材料分子中的原子全部转变成所需产物,不产生副产物,实现零排放;
(2)当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,据此解答,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态;
(3)根据催化剂能降低反应的活化能;
(4)先根据三段式计算出平衡时各物质的浓度,利用各物质平衡的浓度来计算化学平衡常数,利用转化率定义计算CH3OH的转化率;根据等效平衡的从正向建立和逆向建立,转化率之和100%;根据恒容条件下,充入与反应无关的气体,压强增大,平衡不移动,各物质的浓度不变;
(5)原子经济性反应是原材料分子中的原子全部转变成所需产物,不产生副产物,实现零排放;
解答:解:(1)由图象可以看出反应物总能量大于生成物的总能量,则该反应的正反应为放热反应;反应热=419kJ/mol-510kJ/mol=-91 kJ/mol;
故答案为:放热;-91 kJ/mol;
(2)A.随反应进行气体的物质的量增大,压强增大,容器中压强不变,说明到达平衡状态,故A正确;
b.反应达到平衡状态时,各物质的浓度不变,混合气体中c(CO)不变说明到达平衡状态,故B正确;
c.不同物质表示的速率之比等于化学计量数之比,说明到达平衡状态,而v正(H2)=v逆(CH3OH)不等于化学计量数之比,未达平衡状态,故C正确;
d.反应始终按CO与氢气物质的量之比为1:1进行,c(H2)=c(CO)不能说明到达平衡,故D错误;
故答案为;AB;
(3)催化剂能降低反应的活化能,所以图中曲线b表示使用催化剂时反应的能量变化,故选:b;
(4)CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
开始(mol/L) 1 3 0 0
转化(mol/L) 0.5 1.5 0.5 0.5
平衡(mol/L) 0.5 1.5 0.5 0.5
则化学平衡常数K=
=
;
平衡时CH3OH的转化率为
×100%=50%,若开始时充入2mol CH3OH(g) 和2mol H2O(g)达到相同平衡与原平衡等效且等同,c(CO2)=0.5mol/L,转化率之和100%,所以平衡时CH3OH的转化率50%;恒容条件下,充入与反应无关的气体,压强增大,平衡不移动,各物质的浓度不变,c(CO2)=0.5mol/L,
故答案为:
;50%;0.5mol/L;
(5)由题干中原材料分子中的原子全部转变成所需产物,不产生副产物,实现零排放,可知生成物质能有一种,即属于化合反应,反应物为多种,生成物为一种,故选:I;
故答案为:放热;-91 kJ/mol;
(2)A.随反应进行气体的物质的量增大,压强增大,容器中压强不变,说明到达平衡状态,故A正确;
b.反应达到平衡状态时,各物质的浓度不变,混合气体中c(CO)不变说明到达平衡状态,故B正确;
c.不同物质表示的速率之比等于化学计量数之比,说明到达平衡状态,而v正(H2)=v逆(CH3OH)不等于化学计量数之比,未达平衡状态,故C正确;
d.反应始终按CO与氢气物质的量之比为1:1进行,c(H2)=c(CO)不能说明到达平衡,故D错误;
故答案为;AB;
(3)催化剂能降低反应的活化能,所以图中曲线b表示使用催化剂时反应的能量变化,故选:b;
(4)CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
开始(mol/L) 1 3 0 0
转化(mol/L) 0.5 1.5 0.5 0.5
平衡(mol/L) 0.5 1.5 0.5 0.5
则化学平衡常数K=
| 0.5 × 0.5 |
| 0.5×1.53 |
| 4 |
| 27 |
平衡时CH3OH的转化率为
| 1.5 |
| 3 |
故答案为:
| 4 |
| 27 |
(5)由题干中原材料分子中的原子全部转变成所需产物,不产生副产物,实现零排放,可知生成物质能有一种,即属于化合反应,反应物为多种,生成物为一种,故选:I;
点评:本题主要考查反应热的计算、化学平衡的计算、化学平衡的判断、平衡常数、等效平衡等,难度中等,注意基础知识的掌握,注意(4)中对等效平衡规律的掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
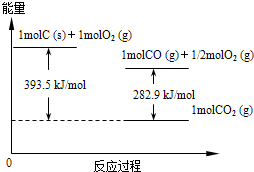 (2012?红桥区一模)能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
(2012?红桥区一模)能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.