题目内容
(8分)用如图所示装置进行下列实验。
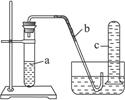
(1)在检查装置气密性后,向试管a中加入10 mL 6 mol·L-1稀硝酸和1 g铜片,立即将带有导管的橡皮塞塞紧管口。请写出试管a中有可能发生的所有反应的化学方程式________________________________________。
(2)该实验刚开始速率缓慢,随后逐渐加快,这是由于_______________________________。
(3)为了使产生的气体不至于逸散到空气中,请写出向试管a中加入试剂的操作方法______________________________________________________________________________。
(4)欲较快地制取NO,可采取的措施有(列举两种)_________________________________、________________________________________。

(1)在检查装置气密性后,向试管a中加入10 mL 6 mol·L-1稀硝酸和1 g铜片,立即将带有导管的橡皮塞塞紧管口。请写出试管a中有可能发生的所有反应的化学方程式________________________________________。
(2)该实验刚开始速率缓慢,随后逐渐加快,这是由于_______________________________。
(3)为了使产生的气体不至于逸散到空气中,请写出向试管a中加入试剂的操作方法______________________________________________________________________________。
(4)欲较快地制取NO,可采取的措施有(列举两种)_________________________________、________________________________________。
(1)3Cu+8HNO3====3Cu(NO3)2+2NO↑+4H2O 2NO+O2====2NO2
(2)铜与硝酸反应为放热反应,随着反应的进行,放出的热量使溶液的温度升高,反应加快
(3)先向试管a中加入10 mL 6 mol·L-1稀硝酸,然后将试管倾斜,将铜片放在试管内壁上方不致滑下,塞上插有导管的塞子,再将试管慢慢直立
(4)将反应物稍微加热、加入相对较浓的硝酸、用铜粉代替铜片等(任写2种,其他合理答案同样给分)
(2)铜与硝酸反应为放热反应,随着反应的进行,放出的热量使溶液的温度升高,反应加快
(3)先向试管a中加入10 mL 6 mol·L-1稀硝酸,然后将试管倾斜,将铜片放在试管内壁上方不致滑下,塞上插有导管的塞子,再将试管慢慢直立
(4)将反应物稍微加热、加入相对较浓的硝酸、用铜粉代替铜片等(任写2种,其他合理答案同样给分)
此题综合考查了硝酸的性质,并和反应速率结合起来。铜与浓硝酸反应生成NO2,与稀硝酸反应生成NO,为使反应速率加快,可适当增加硝酸的浓度;由于此反应放热,速率逐渐加快,也可适当加热使反应加快,因硝酸易分解,因此只能微热。

练习册系列答案
相关题目
 2和稀盐酸共热来制取氯气
2和稀盐酸共热来制取氯气