题目内容
对于反应3Cl2+6NaOH ==5NaCl+NaClO3+3H2O,以下叙述正确的是
- A.Cl2是氧化剂,NaOH是还原剂
- B.被氧化的Cl原子和被还原的Cl原子的物质的量的比为5∶1
- C.Cl2只是还原剂
- D.每生成1mol的NaClO3转移5mol的电子
D
由3Cl2+6NaOH ==5NaCl+NaClO3+3H2O化合价变化知,6个Cl原子,一个从0价变为+5价,5个从0价变为—1价,知Cl2既是氧化剂又是还原剂,A、C均错误;被氧化的Cl原子和被还原的Cl原子的物质的量的比为1∶5,B错误;答案选D。
由3Cl2+6NaOH ==5NaCl+NaClO3+3H2O化合价变化知,6个Cl原子,一个从0价变为+5价,5个从0价变为—1价,知Cl2既是氧化剂又是还原剂,A、C均错误;被氧化的Cl原子和被还原的Cl原子的物质的量的比为1∶5,B错误;答案选D。

练习册系列答案
相关题目
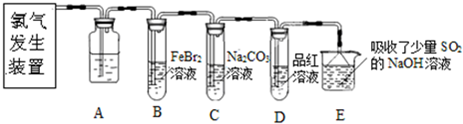
 5NaCl+NaClO3+3H2O,以下叙述正确的是
5NaCl+NaClO3+3H2O,以下叙述正确的是