题目内容
如图装置中,A、B两池溶液的体积均为200mL,
(1)判断装置的名称:A池为______ B池为______
(2)A池中左边石墨棒为______极,电极反应式为______
A池中电池总反应式______
(3)若工作一段时间后,B池中Cu棒上析出224ml气体(标准状态),则电路中通过了______mol电子,B池中溶液质量______(填“增加”、“不变”或“减少”)______ g,若反应前后溶液的体积不变,反应后A池溶液的pH为______.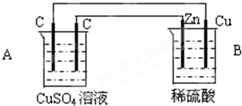
(1)判断装置的名称:A池为______ B池为______
(2)A池中左边石墨棒为______极,电极反应式为______
A池中电池总反应式______
(3)若工作一段时间后,B池中Cu棒上析出224ml气体(标准状态),则电路中通过了______mol电子,B池中溶液质量______(填“增加”、“不变”或“减少”)______ g,若反应前后溶液的体积不变,反应后A池溶液的pH为______.

(1)B装置能自发的进行氧化还原反应,所以B是原电池,则A是电解池,
故答案为:电解池,原电池;
(2)B中锌作负极,铜作正极,则A中左边碳棒是阳极,右边碳棒是阴极,阳极上氢氧根离子放电生成氧气,电极反应式为:4OH--4e-=2H2O+O2↑,阴极上铜离子放电生成铜,所以电池反应式为:2H2O+2CuSO4=2Cu+O2↑+2H2SO4,
故答案为:阳,4OH--4e-=2H2O+O2↑,2H2O+2CuSO4=2Cu+O2↑+2H2SO4;
(3)B中铜棒上电极反应式为:2H++2e-=H2,根据电极反应式知,转移电子的物质的量=
×2=0.02mol,B池中进入的是锌离子,出来的是氢气,转移相同的电子时,进入的质量大于出来的质量,所以溶液质量增加,增加的质量=
×(65-3)g/mol=0.63g,2H2O+2CuSO4=2Cu+O2↑+2H2SO4 知,当转移0.02mol电子时,生成的硫酸中氢离子的物质的量=
×2×2=0.02mol,则氢离子浓度=
=0.1mol/L,所以其ph=1,
故答案为:0.02,增加,0.63,1.
故答案为:电解池,原电池;
(2)B中锌作负极,铜作正极,则A中左边碳棒是阳极,右边碳棒是阴极,阳极上氢氧根离子放电生成氧气,电极反应式为:4OH--4e-=2H2O+O2↑,阴极上铜离子放电生成铜,所以电池反应式为:2H2O+2CuSO4=2Cu+O2↑+2H2SO4,
故答案为:阳,4OH--4e-=2H2O+O2↑,2H2O+2CuSO4=2Cu+O2↑+2H2SO4;
(3)B中铜棒上电极反应式为:2H++2e-=H2,根据电极反应式知,转移电子的物质的量=
| 0.224L |
| 22.4L/mol |
| 0.224L |
| 22.4L/mol |
| 0.02mol |
| 4 |
| 0.02mol |
| 0.2L |
故答案为:0.02,增加,0.63,1.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
 如图装置中,A、B两池溶液的体积均为200mL,
如图装置中,A、B两池溶液的体积均为200mL,

