题目内容
【题目】甲、乙两元素原子的L层电子数都是其他层电子总数的2倍,甲的原子半径大于乙的原子半径,下列说法正确是( )
A. 甲、乙处于同一周期 B. 它们中有一种元素位于第ⅥA族
C. 乙的最高价氧化物与甲的单质不反应 D. 简单甲离子的电子式为:Mg2+
【答案】D
【解析】甲、乙两化合物的核外电子为2、4和2、8、2的一种,根据甲的原子半径大,则甲为Mg元素,乙为C元素。
A. 两者不同周期,A错误;B. C元素位于ⅣA周期,B错误;C. 二氧化碳与镁反应,化学方程式为:2Mg+CO2=2MgO+C,属于置换反应,C错误;D. 正确。故选择D。

练习册系列答案
相关题目
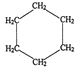
【题目】环丙烷可作为全身麻醉剂,环己烷是重要的有机溶剂。下面是部分环烷烃及烷烃衍生物的结构简式、键线式和某些有机化合物的反应式(其中Pt、Ni是催化剂,且催化性能相当)。
结 构 简 式 |
|
|
|
键 线 式 |
|
|
|
①![]()
②![]()
③![]()
④![]() (未配平)
(未配平)
回答下列问题:
(1)1,4-丁二醇(HOCH2CH2CH2CH2OH)的键线式可以表示为_______________
咔唑( )的分子式为__________________。
)的分子式为__________________。
(2)从反应①~③可以看出,最容易发生开环加成反应的环烷烃是_____________(填名称)。判断的依据为____________________。
(3)写出鉴别环丙烷和丙烯的一种方法。试剂__________;现象与结论__________。
(4)已知某烯烃在酸性高锰酸钾的作用下只产生一种有机物C3H6O,其产物物质的量是原烯烃的两倍且其氢核磁共振谱图只有一个峰。根据题给信息判断该烯烃的结构简式为:__________。