题目内容
【题目】某温度时,在一个2 L的密闭容器中,X、Y、Z(均为气体)三种物质的物质的量随时间变化的曲线如图所示。根据图中数据填空:
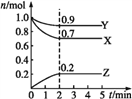
(1)该反应的化学方程式为___________________________。
(2)2 min时反应达到平衡,此时体系内压强与开始时的压强之比为________。
达到平衡时,容器内混合气体的平均相对分子质量比起始时____(填增大、减小或相等)。
(4)若要加快该反应的速率,可以采取的措施有(_____)
A.扩大密闭容器的体积 B.适当升高温度 C.加入正催化剂 D.减小Y的用量
(5)已知该反应为放热反应,2 min后,若要使平衡正向移动,可以采取的措施有(_________)
A.缩小密闭容器的体积 B.适当降低温度 C.加入正催化剂 D.增大Z的用量
【答案】 3X+Y![]() 2Z 9:10 增大 BC AB
2Z 9:10 增大 BC AB
【解析】(1)根据图像可知反应进行到2min时物质的量不再发生变化,此时X减少0.3mol,Y减少0.1mol,Z增加0.2mol,因此该反应的化学方程式为3X+Y![]() 2Z。(2)压强之比是物质的量之比,2 min时反应达到平衡,此时体系内压强与开始时的压强之比为
2Z。(2)压强之比是物质的量之比,2 min时反应达到平衡,此时体系内压强与开始时的压强之比为![]() 。(3)正反应体积减小,混合气体的质量不变,因此达到平衡时,容器内混合气体的平均相对分子质量比起始时增大。(4)A.扩大密闭容器的体积压强减小,反应速率减小,A错误;B.适当升高温度加快反应速率,B正确;C.加入正催化剂加快反应速率,C正确;D.减小Y的用量,浓度减小,反应速率减小,D错误,答案选BC;(5)A.正反应体积减小,缩小密闭容器的体积压强增大,平衡向正反应方向进行,A正确;B.正反应放热,适当降低温度,平衡向正反应方向进行,B正确;C.加入正催化剂不改变平衡状态,C错误;D.增大Z的用量,Z的浓度增大,平衡向逆反应方向进行,D错误,答案选AB。
。(3)正反应体积减小,混合气体的质量不变,因此达到平衡时,容器内混合气体的平均相对分子质量比起始时增大。(4)A.扩大密闭容器的体积压强减小,反应速率减小,A错误;B.适当升高温度加快反应速率,B正确;C.加入正催化剂加快反应速率,C正确;D.减小Y的用量,浓度减小,反应速率减小,D错误,答案选BC;(5)A.正反应体积减小,缩小密闭容器的体积压强增大,平衡向正反应方向进行,A正确;B.正反应放热,适当降低温度,平衡向正反应方向进行,B正确;C.加入正催化剂不改变平衡状态,C错误;D.增大Z的用量,Z的浓度增大,平衡向逆反应方向进行,D错误,答案选AB。