题目内容
(2分)已知常温下,氨水中NH3·H2O的电离平衡常数:K=1.6×10-5;若NH3·H2O的起始浓度为1mol·L-;则平衡时c(OH-)=
(2分)4×10 -3mol·L-1 (不带单位扣1分)
根据电离平衡常数的表达式可知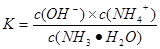 ,c(OH-)=
,c(OH-)=
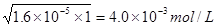 。
。
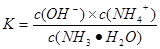 ,c(OH-)=
,c(OH-)=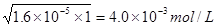 。
。
练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
题目内容
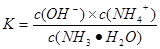 ,c(OH-)=
,c(OH-)=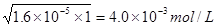 。
。
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案