题目内容
15.下列A、B、C、D是中学常见的混合物分离或提纯的基本装置.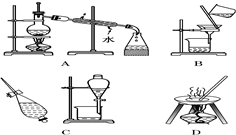
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置.将A、B、C、D 填入适当的空格中.
(1)从碘水中提取碘C(或CA);
(2)分离酒精与水的混合物A;
(3)分离植物油和水C;
(4)除去粗盐中的泥沙制精盐BD.
分析 (1)碘不易溶于水,易溶于有机溶解;
(2)酒精与水互溶,但沸点不同;
(3)植物油和水分层;
(4)泥沙不溶于水.
解答 解:(1)碘不易溶于水,易溶于有机溶解,则利用有机溶剂萃取后分液,再蒸馏得到碘,选择装置为C(或CA),故答案为:C(或CA);
(2)酒精与水互溶,但沸点不同,则蒸馏分离,选择装置为A,故答案为:A;
(3)植物油和水分层,则分液可分离,选择装置为C,故答案为:C;
(4)泥沙不溶于水,则过滤后蒸发可得到精盐,选择装置为BD,故答案为:BD.
点评 本题考查混合物分离提纯实验,为高频考点,侧重于学生的分析能力和实验能力的考查,注意分离原理及实验中的装置、仪器是解答本题的关键为解答的关键,题目难度不大.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
6.既有离子键又有共价键的化合物是( )
| A. | NH4NO3 | B. | NaCl | C. | H2SO4 | D. | H2O |
10.500mL含有MgCl2、NaCl、Na2SO4三种物质的混合溶液,已知其中含有Cl-为1.8mol,Na+为2mol,Mg2+为0.5mol,则SO42-的物质的量浓度为( )
| A. | 0.6mol/L | B. | 0.7mol/L | C. | 1.2mol/L | D. | 1.0mol/L |
20.用NA表示阿伏德罗常数,下列叙述正确的是( )
| A. | 常温常压下,32g氧气所含的原子数目为2NA | |
| B. | 标准状况下,22.4LH2O含有的分子数为NA | |
| C. | 5.6gFe和足量的盐酸反应时,失去的电子数为0.3NA | |
| D. | 0.5mol/L的MgCl2溶液中,含有Cl-个数为NA |
4.1.28g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为( )
| A. | 64g | B. | 64 | C. | 64 g/mol | D. | 32 g/mol |
5.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 1molNaCl固体溶于1L水所得溶液中NaCl的物质的量浓度为1mol•L-1 | |
| B. | 常温常压下,11.2L H2所含的原子数目小于NA | |
| C. | 0.5mol/L的MgCl2溶液中,含有Cl-个数为NA | |
| D. | 在钠与氯气的反应中,1mol钠失去电子的数目为2NA个 |
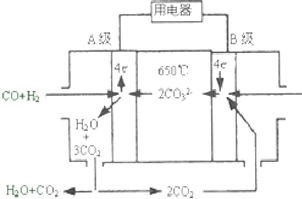 熔融碳酸盐燃料电池(MCFS),发明于1889年.现有一个碳酸盐燃料电池,以一定比例Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1:1)直接作燃料,其工作原理如图所示.请回答下列问题:
熔融碳酸盐燃料电池(MCFS),发明于1889年.现有一个碳酸盐燃料电池,以一定比例Li2CO3和Na2CO3低熔混合物为电解质,操作温度为650℃,在此温度下以镍为催化剂,以煤气(CO、H2的体积比为1:1)直接作燃料,其工作原理如图所示.请回答下列问题: