��Ŀ����
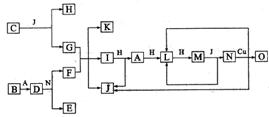
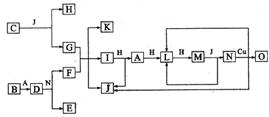
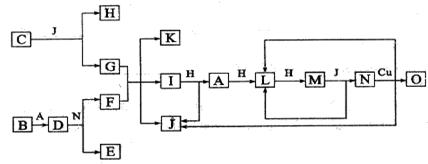
��֪A��O������һ�����ʣ���O���������ʾ��ɶ�����Ԫ����ɣ�����֮���ת����ϵ����ͼ��ʾ����Ӧ�����ԣ���A��B��H�ֱ��ǵ��ʡ�B����ˮ������Ӧ�����ˮѸ�ٷ�Ӧ���ų�������D��һ�����ӻ�������������ӵĸ����� Ϊ2�U3��������ˮ����Ӧ�õ����ּCΪ����ɫ���廯���O����G��ˮ��Һ��Ӧ������ɫ�� ����
��ش��������⣺��1�����B���ʵ�Ԫ��λ�����ڱ��� ���ڣ��� �塣������C��D�ĵ���ʽΪ ___ ��_____________��
��2��J�ķе�������⣨H2Se���ķе�ߣ���ԭ���� ��
��3��д��I��H�ڵ�ȼ�����·�Ӧ����A��J�Ļ�ѧ����ʽ��
��4��д��D��������N��Ӧ����E��F�Ļ�ѧ����ʽ�� ��
д��G��F���ȷ�Ӧ����K��I��J�Ļ�ѧ����ʽ�� ��
��5����ͼ����ͬһ��Ӧ��һ����������������������ԭ���������ķ�Ӧ���� ����
��1���� II A 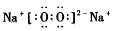
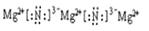
��2��ˮ����֮��������
��3��4NH3��3O2 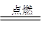 2N2��6H2O
2N2��6H2O
��4��Mg3N2��8HNO3 = Mg(NO3)2��2 NH4NO3
NH4NO3+NaOH NH3��+NaNO3+H2O
NH3��+NaNO3+H2O
��5��2
�������������B����ˮ������Ӧ�����ˮѸ�ٷ�Ӧ���ų�������˵��B��Mg��D��һ�����ӻ�������������ӵĸ�����Ϊ2�U3��������ˮ����Ӧ�õ����ּ˵��D��Mg3N2��CΪ����ɫ���廯���˵��CΪNa2O2������Щ������ϵͼ�����ο����Ƴ�A��N2��B:Mg, C:Na2O2 ,D��Mg3N2, E:Mg(NO3)2, F:NH4NO3, G:NaOH, H:O2, I:NH3, J:H2O, K:NaNO3, L:NO , N:HNO3, M:NO2, O:Cu(NO3)2.
��1��Mg��12��Ԫ�أ�λ�����ڱ��ĵ������ڵ�II���塣
��2��H2O�ķе��H2Se�ߣ�����Ϊ�����������ԭ��
��3�������������е�ȼ�����ɵ�����ˮ��
��4������þ�����ᷴӦ����������þ������泥�����狀����������м��ȣ����ɰ����������ƺ�ˮ��
��5��������������C+J��Ӧ�У���Ԫ�صı仯����M+J��Ӧ�У���Ԫ�صı仯��
���㣺����Ԫ�����ʼ��ת��
���������⿼���˵�Ԫ�ؼ����ʵ�ת�����漰�������͵ķ�Ӧ���ۺ��Խ�ǿ���ѶȽϴ�ѧ��Ҫ���۳������ʵ��������ʣ��Ա��ܸ��õĴ��������⡣



 ��������ͼ�ش���������(ͼ��A��B��C��D��E������һ���л���)��
��������ͼ�ش���������(ͼ��A��B��C��D��E������һ���л���)��