题目内容
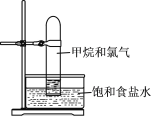
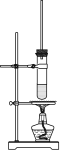
【题目】某同学利用下图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质。

请回答下列问题。
(1)硬质试管中发生的化学方程式___________________。
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色,则说明硬质试管中固体物质一定有_________,可能有_________(填写“化学式”),若溶液未变红色,则说明硬质试管中固体物质的成分是___________________(填写“化学式”)。

(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是:______(用离子方程式表示)。
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与上述白色沉淀变成红褐色的反应的化学方程式____________________________。
(5)一段时间后,该同学发现(3)中未变红的溶液变成红色,说明Fe2+具有_____性。由此可知,实验室中含Fe2+的盐溶液现用现配制的原因是_________,并且配制含Fe2+的盐溶液时应加入少量_____________。
【答案】3Fe+4H2O(g)![]() Fe3O4+4H2 Fe3O4 Fe Fe3O4和Fe Fe+2Fe3+=3Fe2+ 4Fe(OH)2+O2+2H2O=4Fe(OH)3 还原 Fe2+易被空气中的氧气氧化而变质 铁粉或铁屑
Fe3O4+4H2 Fe3O4 Fe Fe3O4和Fe Fe+2Fe3+=3Fe2+ 4Fe(OH)2+O2+2H2O=4Fe(OH)3 还原 Fe2+易被空气中的氧气氧化而变质 铁粉或铁屑
【解析】
(1)铁粉与水蒸气反应,生成Fe3O4和H2;
(2)KSCN遇到Fe3+后迅速出现血红色,利用该方法检验Fe3+;
(3)铁粉能将Fe3+还原为Fe2+;
(4)滴入NaOH溶液后,Fe(OH)2白色沉淀逐渐变为灰绿色,最终变为红褐色的Fe(OH)3;
(5)铁粉能将Fe3+还原为Fe2+,Fe2+具有还原性,Fe2+易被空气中的O2氧化。
(1)铁粉与水蒸气反应,生成Fe3O4和H2,反应方程式为3Fe+4H2O(g) ![]() Fe3O4+4H2;
Fe3O4+4H2;
(2)取少量溶液B滴加KSCN溶液,若溶液变红色,说明硬质试管中固体物质一定有Fe3O4,可能含有Fe,若溶液未变红色,说明硬质试管中固体物质的成分是Fe3O4和Fe;
(3)铁粉能将Fe3+还原为Fe2+,离子方程式为:Fe+2Fe3+=3Fe2+;
(4)试管中滴入NaOH溶液后,Fe(OH)2白色沉淀逐渐变为灰绿色,最终变为红褐色的Fe(OH)3,发生的反应为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(5)铁粉能将Fe3+还原为Fe2+,Fe2+具有还原性,Fe2+易被空气中的O2氧化,因此实验室中含Fe2+的盐溶液现用现配制,因此配制含Fe2+的盐溶液时应加入少量铁粉或者铁屑,防止Fe2+被氧化。